
25℃,将某一元碱MOH和盐酸等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表,则下列判断不正确的是
实验编号 | c(盐酸)/(mol·L-1) | c(MOH)/(mol·L-1) | 反应后溶液的pH |
甲 | 0.20 | 0.20 | 5 |
乙 | 0.10 | a | 7 |
A.a>0.10
B.实验甲所得溶液:c(Cl-)>c(M+)>c(H+)>c(MOH)
C.将实验甲中所得溶液加水稀释后,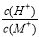 变小
变小
D.MOH的电离平衡常数可以表示为:
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源:2016届江西南昌二中、临川一中等高三4月联考二理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】现有前四周期六种元素X、Y、Z、E、F、G,它们的原子序数依次增大,除G外,其它五种元素都是短周期元素。X、Y、E三种元素组成的化合物是实验室常用燃料。取F的化合物做焰色反应实验,其焰色呈黄色,G的单质是生活中常见的一种金属,GE是黑色固体。请回答下列问题:
(1)写出基态G原子电子排布式: ;Y、Z、E、F、G的第一电离能最大的是 (用元素符号表示)。
(2)X、Y、Z形成3原子分子M,每个原子价层电子均达到稳定结构。M分子的结构式为 。1molM含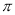 键数目为 。
键数目为 。
(3)根据价层电子对互斥理论(VESPR)推测:ZE2-的立体构型为 ,YE32-的中心原子杂化类型为 。
(4)Z与X形成的简单化合物极易溶解在E与X形成的简单化合物的原因是________。
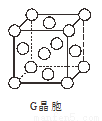
(5)G晶胞结构如图所示。已知立方体的棱长为apm,G 晶体密度为bg·cm-3,则阿伏加德罗常数NA= (用含a、b的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏六盘山高中高一下期中化学试卷(解析版) 题型:选择题
下列措施不符合节能减排、绿色发展理念的是
A.大力发展火力发电,解决电力紧张问题
B.在屋顶安装太阳能热水器为居民提供生活用热水
C.尽量少开私家车,多骑自行车
D.用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气
查看答案和解析>>
科目:高中化学 来源:2016届海南海南中学高三考前模拟十一化学试卷(解析版) 题型:选择题
按表中所述内容进行实验,可以实现相应的实验目的的是( )
选项 | 甲中试剂 | 乙中试剂 | 气体成份及实验目的 |
|
A | NaHSO3溶液 | 硅酸钠溶液 | HCl:证明非金属Cl>S>Si | |
B | FeI2淀粉溶液 | KSCN溶液 | Cl2:验证氧化性Cl2>Fe3+>I2 | |
C | 溴水 | AgNO3溶液 | 乙烯:验证溴水与乙烯发生的是加成反应 | |
D | Ba(OH)2溶液 | 品红溶液 | .验证混合气体中含有SO2和CO2 |
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第五次适应性考试理综化学试卷(解析版) 题型:实验题
【化学——选修5:有机化学基础】
白藜芦醇是一种抗肿瘤的药物,合成它的一种路线如下:
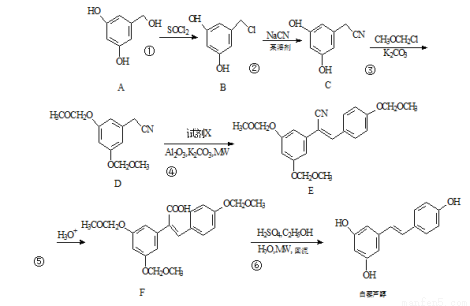
(1)化合物F中的含氧官能团的名称是________和________。
(2)③的反应类型是________________
(3)反应④中加入试剂X的分子式为C9H10O3,X的结构简式为________________。
(4)1mol白藜芦醇最多能与____molH2反应,与浓溴水反应时,最多消耗____molBr2。
(5)D的一种同分异构体满足下列条件:
Ⅰ. 属于α?氨基酸
Ⅱ. 能使溴水褪色,但不能使FeCl3溶液显色
Ⅲ. 分子中有7种不同化学环境的氢,且苯环上的一取代物只有一种
写出该同分异构体的结构简式:________________。(任写一种)
(6)根据已有知识并结合相关信息,写出以乙醇为原料制备CH3CH===C(CH3)CN的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三第五次适应性考试理综化学试卷(解析版) 题型:选择题
化学与生活、生产密切相关,下列说法正确的是
A.对“地沟油”进行分馏可得到汽油
B.PM2.5、CO2都属于空气质量日报的内容
C.硅酸多孔、吸水能力强,常用作袋装食品的干燥
D.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古包头九中高一下第一次月考化学试卷(解析版) 题型:选择题
一定量Fe和Fe2O3的混合物投入250ml 2mol/L的硝酸中,反应共生成1.12L NO(标准状况下),再向反应后的溶液中加入1mol/L的硝酸NaOH溶液,当沉淀完全时所加NaOH溶液的体积最少是
A.450ml B.500ml C.400ml D.不能确定
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下期中化学试卷(解析版) 题型:填空题
能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)氢气在O2中燃烧的反应是______热反应(填“放”或“吸”),这是由于反应物的总能量______生成物的总能量(填“大于”、“小于”或“等于”,下同);
(2)从化学反应的本质角度来看,是由于断裂反应物中的化学键吸收的总能量______形成产物的化学键放出的总能量.已知破坏1mol H-H键、1mol O=O键、1mol H-O键时分别需要吸收436kJ、498kJ、463kJ的能量。则2mol H2(g)和1mol O2(g)转化为2mol H2O(g)时放出的热量为 。

(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置(其中电解质溶液为KOH溶液),被称为氢氧燃料电池.该电池的正极是______
(填a电极或b电极),负极反应式为______。
(4)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,已知正极上
发生的电极反应式为:O2+4e-===2O2-则负极上发生的电极反
应式为________;电子从该极________(填“流入”或“流出”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一下期中化学试卷(解析版) 题型:填空题
Ⅰ、一定温度下,在容积为VL的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中a/b=_
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:_
(3)下列叙述中能说明上述反应达到平衡状态的是_
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
Ⅱ、某研究性学习小组为探究铁与盐反应,取同质量、体积的铁片、同浓度盐酸做了下列平行实验:
实验①:把纯铁片投入到盛有稀盐酸的试管中,发现氢气发生的速率变化如图所示:

实验②:把纯铁片投入到含FeCl3的同浓度工业稀盐酸中,发现放出氢气的量减少。
实验③:在盐酸中滴入几滴CuCl2溶液,生成氢气速率加快。
试回答下列问题:
(1)试分析实验①中t1~t2速率变化的主要原因是_ ,t2~t3速率变化的主要原因是_ 。
(2)实验②放出氢气的量减少的原因是(用离子方程式表示)_
(3)某同学认为实验③反应速率加快的主要原因是因为形成了原电池,你认为是否正确?_ (填“正确”或“不正确”)。请选择下列相应的a或b作答。
a、若不正确,请说明原因:_
b、若正确则写出实验②中原电池的正、负极电极反应式_
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com