
某光卤石(KCl·MgCl2·6H2O)样品中含有不和NaOH溶液、盐酸反应的杂质.为测定样品中KCl·MgCl2·6H2O的质量分数.有如下操作:
①称取a g样品,放入锥形瓶中加适量水溶解.
②往锥形瓶中加入b mol·L-1的NaOH溶液100 mL(过量),振荡.
③过滤并冲洗沉淀2~3次,收集滤液及洗液于锥形瓶中.
④往沉淀中滴加c mol·L-1的稀HCl溶液至沉淀溶解,消耗盐酸V1 mL.
⑤用c mol·L-1的盐酸滴定过量的NaOH至终点,消耗盐酸V2 mL.
⑥向步骤②锥形瓶中加入指示剂2~3滴.
⑦向步骤③锥形瓶中加入指示剂2~3滴.
回答:
(1)正确且必要的操作顺序是________(填序号).
(2)KCl·MgCl2·6H2O质量分数是________.
科目:高中化学 来源: 题型:
请根据提供的实验试剂和仪器(所需的仪器任选),选择精确度较高的实验方案,简要写出第二步以后的实验步骤和实验结果。
一、可选用的实验试剂:
(1)a mol·L-1的NaOH溶液
(2)b mol·L-1的Na2CO3溶液
(3)c mol·L-1的HCl溶液
(4)d mol·L-1的AgNO3溶液
(5)酚酞试液
(6)紫色石蕊试液
二、实验步骤:
第一步:称取m g样品,放入250 mL烧杯中,加适量水溶解;
第二步:……
三、计算样品中KCl·MgCl2·6H2O的质量分数表达式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)可供选用的试剂;
①a mol·L-1 NaOH溶液 ②b mol·L-1Na2CO3溶液 ③c mol·L-1盐酸 ④d mol·L-1 AgNO3溶液 ⑤甲基橙 ⑥酚酞
(2)实验步骤
第一步:称取m g样品,放入250 mL烧杯中,加适量水溶解;
第二步:_______________________________________________________;
第三步:_______________________________________________________;
第四步:_______________________________________________________。
(3)计算样品中KCl·MgCl2·6H2O质量分数的表达式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某光卤石(KCl·MgCl2·6H2O)样品中含有不跟NaOH溶液和盐酸反应的杂质,某校化学课外活动研究小组现欲测定此样品中含KCl·MgCl2·6H2O的质量分数,经讨论有多种实验测定方案。
请根据提供的实验试剂和仪器(所需的仪器任选),选择精确度较高的实验测定方案,简要写出第二步以后的实验步骤和实验结果。
一、可选用的实验试剂:
(1)![]() mol·L
mol·L![]() NaOH溶液 (2)
NaOH溶液 (2)![]() mol·L
mol·L![]() Na2CO3溶液 (3)c mol·L
Na2CO3溶液 (3)c mol·L![]() HCl溶液
HCl溶液
(4)d mol·L![]() AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
AgNO3溶液 (5)酚酞试液 (6)甲基橙试液
二、实验步骤:
第一步:称取m g样品,放入250mL烧杯中,加适量水溶解
第二步:
计算样品中含KCl·MgCl2·6H2O(相对分子质量为277.5)的质量分数的表达式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(10分)江苏省拥有丰富的海洋资源,盐化工是连云港市的主要产业之一。从盐卤初步得到的光卤石(KCl?MgCl2?6H2O)晶体中,还含有约8%的NaCl。
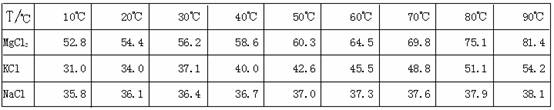
![]() 为了从光卤石中提取KCl和MgCl2,某学习小组查阅资料得到MgCl2、KCl和NaCl在不同温度下的溶解度S(g/100g水)的数据如下:
为了从光卤石中提取KCl和MgCl2,某学习小组查阅资料得到MgCl2、KCl和NaCl在不同温度下的溶解度S(g/100g水)的数据如下:
 |
![]()
![]()
![]()
![]()
![]()
并设计出下面的实验流程:w.w.w.k.s.5.u.c.o.m
![]()

![]()
![]()
![]()
![]()
根据他们提供的数据和实验回答下列问题:
![]() 问题1:以上实验流程中晶体X的化学式为 ,若制得的X还含有少量的可溶性杂质,可用 的方法进一步提纯。操作步骤①中为趁热过滤的原因是 。
问题1:以上实验流程中晶体X的化学式为 ,若制得的X还含有少量的可溶性杂质,可用 的方法进一步提纯。操作步骤①中为趁热过滤的原因是 。
问题2:工业上采用电解无水氯化镁的方法制取金属镁。
(1)若在空气中加热MgCl2?6H2O,生成的是Mg(OH)Cl,写出反应的化学方程式:
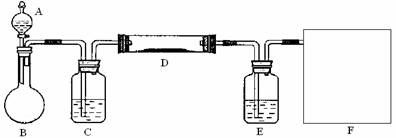
(2)该小组同学采取将浓硫酸滴入浓盐酸制取氯化氢气体的方法,用下图的实验装置,在干燥的HCl气流中加热MgCl2?6H2O来得到无水MgCl2。装置中盛有浓硫酸的仪器分别是 (填写仪器的符号),需要加热的仪器是 (同上)。
(3)为防止对环境的污染,还需要将尾气吸收,但实验室现有的仪器和试剂只有:烧杯、导管、蒸馏水、酒精、苯、四氯化碳。请你为他们设计一个尾气的吸收装置,将装置图画在方框内并在图中标明所用试剂。
问题3:MgO则是重要的耐火材料。在550℃时,MgCl2?6H2O会分解生成MgO、MgCl2、HCl和水,若不补充其它原料,使一定量的MgCl2?6H2O全部生成a mol MgO、b mol MgCl2和36.5%的盐酸,则 a∶b≈_______(取整数值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com