

分析 右室中混合气体总物质的量不变,平衡时左室与右室压强相等,温度、压强相同条件下,体积之比等于气体物质的量之比,降低温度由平衡(I)向平衡(II)移动,左室中体积减小,则左室中混合气体总物质的量减小,说明左室中降低温度平衡向右移动;
利用体积之比等于物质的量的之比,则平衡I左室中气体总物质的量为2mol×$\frac{2.8}{2.2}$=$\frac{28}{11}$mol,则:
X(g)+2Y(g)?2Z(g)物质的量减少△n=1
起始量(mol):1 2 0
变化量(mol):$\frac{5}{11}$ $\frac{10}{11}$ $\frac{10}{11}$ 3-$\frac{28}{11}$=$\frac{5}{11}$
平衡量(mol):):$\frac{6}{11}$ $\frac{12}{11}$ $\frac{10}{11}$
再根据平衡常数K=$\frac{{c}^{2}(Z)}{c(X)×{c}^{2}(Y)}$计算.
解答 解:右室中混合气体总物质的量不变,平衡时左室与右室压强相等,温度、压强相同条件下,体积之比等于气体物质的量之比,降低温度由平衡(I)向平衡(II)移动,左室中体积减小,则左室中混合气体总物质的量减小,说明左室中降低温度平衡向右移动,则正反应为放热反应,
利用体积之比等于物质的量的之比,则平衡I左室中气体总物质的量为2mol×$\frac{2.8}{2.2}$=$\frac{28}{11}$mol,则:
X(g)+2Y(g)?2Z(g)物质的量减少△n=1
起始量(mol):1 2 0
变化量(mol):$\frac{5}{11}$ $\frac{10}{11}$ $\frac{10}{11}$ 3-$\frac{28}{11}$=$\frac{5}{11}$
平衡量(mol):):$\frac{6}{11}$ $\frac{12}{11}$ $\frac{10}{11}$
达到平衡(Ⅰ)时X的转化率为$\frac{\frac{5}{11}mol}{1mol}$×100%=45.45%;
平衡常数K=$\frac{{c}^{2}(Z)}{c(X)×{c}^{2}(Y)}$=$\frac{(\frac{5}{11})^{2}}{\frac{3}{11}×(\frac{6}{11})^{2}}$mol/L=2.55mol/L,
故答案为:放热;45.45%;2.55mol/L.
点评 本题考查化学平衡计算,难度中等,注意右室中反应体系的物质的量不变、且左室与右室压强相等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 | |
| B. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| C. | 实验室用排饱和食盐水法收集氯气 | |
| D. | 工业上利用O2与SO2反应制取SO3时通入过量O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol Fe与足量的盐酸反应 | B. | 0.4mol Cu投入到足量的稀硫酸中 | ||
| C. | 0.1mol Al与足量的NaOH溶液反应 | D. | 0.1mol Fe与足量的水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
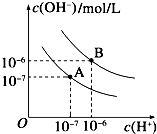 已知水在25℃和95℃时的电离平衡曲线如下图所示:
已知水在25℃和95℃时的电离平衡曲线如下图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管B中放入铁粉和石棉绒的混合物,再结合一些步骤,就可以完成髙温下“Fe与水蒸气的反应实验”(己知石棉绒是耐高温材料,不与水和铁反应).
某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管B中放入铁粉和石棉绒的混合物,再结合一些步骤,就可以完成髙温下“Fe与水蒸气的反应实验”(己知石棉绒是耐高温材料,不与水和铁反应).| 实验步骤 | 预期实验现象与结论 |
| 取反应后干燥的固体于试管中,加入足量的1mol•L-1硫酸溶解 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 只有在t1℃时,NaCl和MgSO4的溶解度才相等 | |
| B. | t1℃~t2℃,MgSO4的溶解度随温度升高而减小 | |
| C. | 在t2℃时,MgSO4饱和溶液的溶质质量分数最大 | |
| D. | 把MgSO4饱和溶液的温度从t3℃降至t2℃时,有晶体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2) | B. | (2)(4) | C. | (2)(5) | D. | (3)(6) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com