
压强/Pa | 4×105 | 6×105 | 1×106 | 2×106 |
D的浓度/mol·L -1 | 0.08 | 0.100 | 0.200 | 0.440 |
(1)压强从4×105 Pa增加到6×105 Pa时,平衡向______反应方向移动(填“正”或“逆”,下同),理由是__________________________________________________。
(2)压强从1×106 Pa增加到2×106 Pa时,平衡向_______反应方向移动。
科目:高中化学 来源: 题型:阅读理解
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+●提出假设: (1)假设①:该混合金属粉末中除镁外还含有 Al Al 元素假设②:该混合金属粉末中除镁外还含有 Zn Zn 元素假设③:该混合金属粉末中除镁外还含有铝、锌元素 ●实验探究: 甲同学基于假设③设计实验方案如下:乙同学同样基于假设③设计另一实验方案如下: 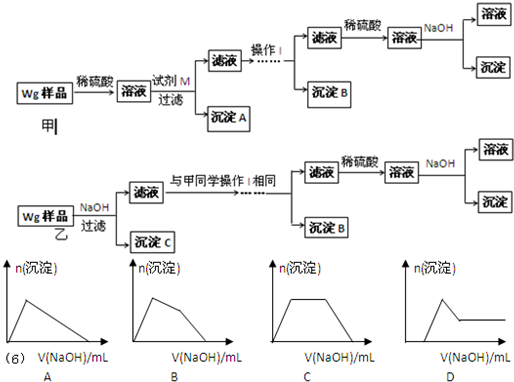 (2)试剂M是 NaOH溶液 NaOH溶液 ;沉淀B是Al(OH)3 Al(OH)3 .(3)丙同学认为乙同学的方案比甲同学的好,理由是 步骤简单,节约试剂 步骤简单,节约试剂 .(4)丁同学研究了甲、乙两同学的方案后,在其中一种方案的基础上用最简便方法测定了Wg样品中金属镁(Mg)的质量,他的方法是 将沉淀C洗涤、小心干燥后称量 将沉淀C洗涤、小心干燥后称量 .(5)操作Ⅰ的主要过程是:在滤液中逐滴加入 稀硫酸 稀硫酸 ,直至生成的沉淀刚好溶解,再加入足量的稀氨水 稀氨水 .(6)某溶液中含有Zn2+、Al3+、NH4+和SO42-等离子,向其中逐滴加入NaOH溶液,则生成沉淀的物质的量与加入NaOH溶液体积关系的图象正确的是 B B .
查看答案和解析>> 科目:高中化学 来源: 题型: 某体积可变的密闭容器中盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B
根据上述数据,完成下列填空:? (1)实验1,反应在10~20 min时间内A的平均反应速率为______________mol·(L·min)-1。 (2)实验2,A的初始浓度c2=_______mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是_____________________。 (3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填“>”“=”或“<”),且c3_______1.0 mol·L-1(填“>”“=”或“<”)。 (4)比较实验4和实验1,可推测该反应是_______(填“吸热”“放热”)反应。理由是_________________________________________________ 。? 查看答案和解析>> 科目:高中化学 来源: 题型:解答题 Ⅰ.某研究性学习小组用10g胆矾制取CuO,并证明CuO可以催化H2O2的分解反应. | ||||||||||||||||||||||||||||||||||||||||||||||
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
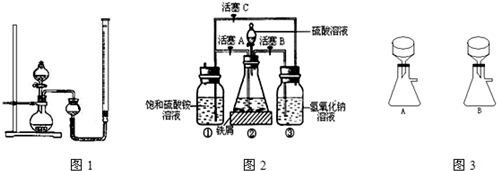
 +5Fe2++8H+=Mn2++5Fe3++4H2O
+5Fe2++8H+=Mn2++5Fe3++4H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 |
| -4 |
查看答案和解析>>
科目:高中化学 来源:2013年天津市红桥区高考化学二模试卷(解析版) 题型:填空题
| 溶解度(S)/g | 溶度积(Ksp) | ||
| Ca(OH)2 | Ba(OH)2 | CaCO3 | BaCO3 |
| 0.16 | 3.89 | 2.9×10-9 | 2.6×10-9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com