
【题目】某溶液中可能含有下列6种离子中的某几种:Cl﹣、SO42﹣、HCO3﹣、Na+、K+、Mg2+ , 所含离子的浓度均相等.为了确认溶液的组成,进行如下实验:取200mL上述溶液,加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g,向沉淀中加入过量的盐酸,有2.33g.关于原溶液组成的结论,不正确的是( )
A.一定存在SO42﹣、HCO3﹣、Mg2+ , 至少存在Na+、K+中的一种
B.为了确定是否存在Cl﹣ , 可向溶液中加入硝酸酸化的硝酸银溶液
C.c(HCO3﹣)=0.05mol/L
D.4.88g沉淀中含有3种成分
【答案】B
【解析】解:加入足量Ba(OH)2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.88g,向沉淀中加入过量的盐酸,有2.33g,可知2.33g沉淀为硫酸钡,则含SO42﹣为 ![]() =0.01mol,可知4.88g沉淀为硫酸钡和其它沉淀的混合物,离子浓度均相等,沉淀若为碳酸钡,则含HCO3﹣ , 碳酸钡的质量为0.01mol×197g/mol=1.97g<4.88g﹣2.33g,则沉淀还含为氢氧化镁,则含Mg2+为=
=0.01mol,可知4.88g沉淀为硫酸钡和其它沉淀的混合物,离子浓度均相等,沉淀若为碳酸钡,则含HCO3﹣ , 碳酸钡的质量为0.01mol×197g/mol=1.97g<4.88g﹣2.33g,则沉淀还含为氢氧化镁,则含Mg2+为= ![]() =0.01mol,由电荷守恒可知,一定含Na+、K+中的一种,不能确定是否含Cl﹣ , 若Na+、K+均存在,则含Cl﹣ , A.由上述分析可知,一定存在SO42﹣、HCO3﹣、Mg2+ , 至少存在Na+、K+中的一种,故A正确;
=0.01mol,由电荷守恒可知,一定含Na+、K+中的一种,不能确定是否含Cl﹣ , 若Na+、K+均存在,则含Cl﹣ , A.由上述分析可知,一定存在SO42﹣、HCO3﹣、Mg2+ , 至少存在Na+、K+中的一种,故A正确;
B.加入硝酸酸化的硝酸银溶液,SO42﹣、Cl﹣均反应生成白色沉淀,不能检验,故B错误;
C.c(HCO3﹣)= ![]() =0.05mol/L,故C正确;
=0.05mol/L,故C正确;
D.由上述分析可知,4.88g沉淀中含有3种成分,分别为硫酸钡、氢氧化镁、碳酸钡,故D正确;
故选B.


科目:高中化学 来源: 题型:
【题目】25℃时,已知H2CO3H++HCO3﹣K1=4.3×l0﹣7;
HCO3﹣H++CO32﹣K2=5.6×l0﹣11;
H2OH++OH﹣Kw=1.0×l0﹣14
现取10.6g Na2CO3与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH 的关系如图所示.下列有关溶液中离子浓度关系叙述正确的是( )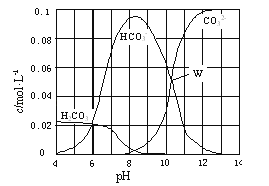
A.W点所示的溶液中:c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣)
B.pH=4的溶液中:c(H2CO3)+c(HCO3﹣)+c(CO32﹣)=0.1 molL﹣1
C.pH=8的溶液中:c(H+)+c(H2CO3)+c(HCO3﹣)=c(OH﹣)+c(Cl﹣)
D.pH=11的溶液中:CO32﹣+H2OHCO3﹣+OH﹣K=1.8×l0﹣4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关热化学方程式及其叙述正确的是( )
A.氢气的燃烧热为﹣285.5kJ/mo1,则电解水的热化学方程式为:2H2O(1)=2H2(g)+O2(g)△H=+285.5kJ/mo1
B.1mol甲烷完全燃烧生成CO2和H2O(1)时放出890kJ热量,则它的热化学方程式为: ![]() CH4(g)+O2(g)=
CH4(g)+O2(g)= ![]() CO2(g)+H2O(1)△H=﹣445kJ/mol
CO2(g)+H2O(1)△H=﹣445kJ/mol
C.已知:2C(s)+O2(g)=2CO(g)△H=﹣221 kJmol﹣1 , 则C的燃烧热为﹣110.5kJ/mo1
D.HF与NaOH溶液反应:H+(aq)+OH﹣(aq)=H2O(1)△H=﹣57.3kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)=2H2O(g)△H13H2(g)+Fe2O3(s)=2Fe(s)+3H2O(g)△H2
2Fe(s)+ ![]() O2(g)=Fe2O3(s)△H3
O2(g)=Fe2O3(s)△H3
2Al(s)+ ![]() O2(g)=Al2O3(s)△H4
O2(g)=Al2O3(s)△H4
2Al(s)+Fe2O3(s)=A12O3(s)+2Fe(s)△H5
下列关于上述反应焓变的判断正确的是( )
A.△H1<0,△H3>0
B.△H5<0,△H4<△H3
C.△H1=△H2+△H3
D.△H3=△H4+△H5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,在研究新能源的前沿技术上,科学家致力于二氧化碳的“组合转化”技术的研究,把过多的二氧化碳转化为有益于人类的物质。
(1)乙烯的产量是衡量一个国家石油化工发展水平的标志之一,下列石油化工生产能提高乙烯的产量的是________。
A.蒸馏、分馏
B.催化裂化
C.催化裂解
D.催化重整
(2)下列说法不正确的是__________。
A.石油是混合物,分馏后得到的馏分是纯净物
B.煤隔绝空气加强热可以得到黑褐色油状的煤焦油
C.煤的气化和液化是使煤变成清洁能源的有效途径
D.从绿色化学角度考虑,以植物为主的生物质资源,是未来的理想资源
(3)如果将CO2和H2以1∶4的比例混合,通入反应器,在适当的条件下反应,可获得一种重要的能源。请完成以下化学方程式:
CO2+4H2→()+2H2O
(4)若将CO2和H2以1∶3的比例混合,使之发生反应生成某种重要的化工原料和水,该原料可能是________。
A.烷烃
B.烯烃
C.炔烃
D.芳香烃
(5)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
原料— 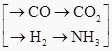 →CO(NH2)2
→CO(NH2)2
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?。
(6)请根据以上信息,设计工业合成尿素的条件。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乳酸(PLA)是以有机酸——乳酸为原料生产的新型聚酯材料,性能胜于现有塑料聚乙烯、聚丙烯、聚苯乙烯等材料,是新世纪最具发展前途的新型包装材料,是环保包装材料中的一颗明星。日本钟纺公司以玉米为原料发酵生产聚乳酸,利用聚乳酸制成生物降解性发泡材料。该材料的强度、缓冲性、耐药性等与聚苯乙烯塑料相同,经焚烧后不污染环境,还可肥田。下列说法不正确的是( )
A.聚乳酸使用后能被自然界中微生物完全降解,最终生成二氧化碳和水,不污染环境
B.聚乳酸适用于吹塑、热塑等各种加工方法,加工方便,应用十分广泛
C.聚乳酸(PLA)是一种天然高分子、对环境友好的聚酯材料
D.聚乳酸是以淀粉发酵(或化学合成)得到的,以乳酸为基本原料制备的一种聚酯材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世博园地区改造前,规划区内有一座大型钢铁厂,附近居民曾饱受到该厂产生的棕红色烟雾的困扰.估计这一空气污染物可能含有( )
A.FeO粉尘
B.Fe3O4粉尘
C.Fe2O3粉尘
D.NO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】防止钢铁的腐蚀是世界级难题,每年全世界钢产量的四分之一因腐蚀而损失
(1)钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中的电极反应式为、。
(2)为降低某水库的铁闸门的被腐蚀速率,可以采用图甲方案,其中焊接在铁闸门上的固体材料R可以采用________。
A.铜
B.钠
C.锌
D.石墨
(3)图乙所示方案也可降低铁闸门的被腐蚀速率,其中铁闸门应该连接在直流电源的极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com