
| A、NaOH、H2SO4 |
| B、CuCl2、Cu(NO3)2 |
| C、Na2SO4、NaCl |
| D、KNO3、AgNO3 |


科目:高中化学 来源: 题型:
 如图为某市售盐酸试剂瓶标签上的部分数据.
如图为某市售盐酸试剂瓶标签上的部分数据.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol硫单质在足量氧气中燃烧,电子转移6mol |
| B、22.4L CO2所含的分子数为NA个 |
| C、6.02×1023个NO分子的物质的量约为1mol |
| D、1mol/L FeCl3溶液中,Fe3+的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
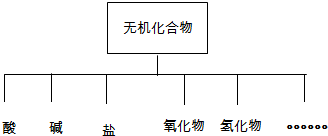
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HNO3 ② |
③NaOH ④ |
⑤Na2SO4 ⑥ |
⑦SO2 ⑧SO3 |
⑨NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含1mol硅原子的SiO2晶体中Si-O键的个数为2NA |
| B、理论上氢氧燃料电池负极消耗11.2L标准状况下气体,外线路通过电子数为NA |
| C、标准状况下,11.2 L氯仿中含有的C-Cl键的数目为1.5NA |
| D、15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
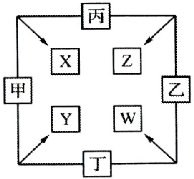 甲、乙、丙、丁均是由短周期元素组成的单质,X、Y、Z、W均为化合物,常温下,X为淡黄色固体,Z遇空气变为红棕色,W能使湿润的红色石蕊试纸变蓝色,工业上常用W来制取Z,其转化关系如图.
甲、乙、丙、丁均是由短周期元素组成的单质,X、Y、Z、W均为化合物,常温下,X为淡黄色固体,Z遇空气变为红棕色,W能使湿润的红色石蕊试纸变蓝色,工业上常用W来制取Z,其转化关系如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com