
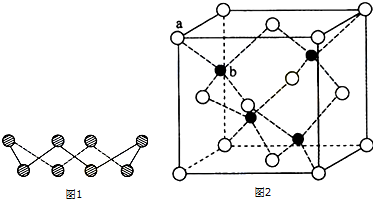
分析 (1)根据图片知,每个S原子含有2个σ键和2个孤电子对,根据价层电子对互斥理论确定S原子杂化方式;
(2)同一主族元素,元素原子失电子能力随着原子序数的增大而增强,原子失电子能力越强,其第一电离能越小;
(3)Se元素34号元素,M电子层上有18个电子,分别位于3s、3p、3d能级上;
(4)非金属性越强的元素,其与氢元素的结合能力越强,则其氢化物在水溶液中就越难电离,酸性就越弱;
根据价层电子对互斥理论确定气态SeO3分子的立体构型、SO32-离子的立体构型;
(5)①第一步电离后生成的负离子,较难再进一步电离出带正电荷的氢离子;
②根据中心元素Se的化合价可以判断电性高低,电性越高,对Se-O-H中O原子的电子吸引越强,越易电离出H+;
(6)利用均摊法计算晶胞中Zn、S原子数目,进而计算晶胞质量,再根据ρ=$\frac{m}{V}$计算晶胞密度;
b位置黑色球与周围4个白色球构成正四面体结构,黑色球与两个白色球连线夹角为109°28′,计算a位置白色球与面心白色球距离,设a位置S2-与b位置Zn2+之间的距离,由三角形中相邻两边、夹角与第三边关系:a2+b2-2abcosθ=c2计算.
解答 解:(1)根据图片知,每个S原子含有2个σ键和2个孤电子对,所以每个S原子的价层电子对个数是4,则S原子为sp3杂化;
故答案为:sp3;
(2)同一主族元素,元素原子失电子能力随着原子序数的增大而增强,原子失电子能力越强,其第一电离能越小,所以第一电离能大小顺序:O>S>Se,故答案为:O>S>Se;
(3)Se元素34号元素,M电子层上有18个电子,分别位于3s、3p、3d能级上,所以其核外M层电子的排布式为3s23p63d10;
故答案为:34;3s23p63d10;
(4)非金属性越强的元素,其与氢元素的结合能力越强,则其氢化物在水溶液中就越难电离,酸性就越弱,非金属性S>Se,所以H2Se的酸性比H2S强,气态SeO3分子中Se原子价层电子对个数是3且不含孤电子对,所以其立体构型为平面三角形,SO32-离子中S原子价层电子对个数=3+$\frac{1}{2}$(6+2-3×2)=4且含有一个孤电子对,所以其立体构型为三角锥形;
故答案为:强;平面三角形;三角锥形;
(5)①第一步电离后生成的负离子,较难再进一步电离出带正电荷的氢离子,故H2SeO3和H2SeO4第一步电离程度大于第二步电离;
故答案为:第一步电离后生成的负离子,较难再进一步电离出带正电荷的氢离子;
②H2SeO3和H2SeO4可表示成(HO)2SeO和(HO)2SeO2,H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,正电性更高,导致Se-O-H中O的电子更向Se偏移,越易电离出H+,H2SeO4比H2SeO3酸性强,
故答案为:H2SeO3和H2SeO4可表示成(HO)2SeO和(HO)2SeO2.H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,正电性更高,导致Se-O-H中O的电子更向Se偏移,越易电离出H+;
(6)晶胞中含有白色球位于顶点和面心,共含有8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,黑色球位于体心,共4个,则晶胞中平均含有4个ZnS,质量为4×(87÷6.02×1023)g,晶胞的体积为(540.0×10-10cm)3,则密度为[4×(87÷6.02×1023)g]÷(540.0×10-10cm)3=4.1g•cm-3;
b位置黑色球与周围4个白色球构成正四面体结构,黑色球与两个白色球连线夹角为109°28′,a位置白色球与面心白色球距离为540.0pm×$\frac{\sqrt{2}}{2}$=270$\sqrt{2}$pm,设a位置S2-与b位置Zn2+之间的距离为y pm,由三角形中相邻两边、夹角与第三边关系:y2+y2-2y2cos109°28′=(270$\sqrt{2}$)2,解得y=$\frac{270.0}{\sqrt{1-cos109°28′}}$,
故答案为:4.1;$\frac{270.0}{\sqrt{1-cos109°28′}}$;
点评 本题考查了较综合,涉及粒子空间构型判断、原子杂化方式判断、元素周期律等知识点,根据价层电子对互斥理论、元素周期律等知识点来分析解答,注意(4)氢化物酸性强弱比较方法,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 数目为NA的一氧化碳分子和0.5 mol甲烷的质量比为7:4 | |
| B. | 标准状况下,22.4 L水中含有水分子的数目为NA | |
| C. | 14 g N2中含有电子的数目为14NA | |
| D. | 2.3g Na完全反应时,转移电子的数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
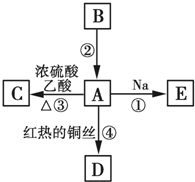 A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示:
A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物质的转化关系如图所示: CH3COOC2H5+H2O
CH3COOC2H5+H2O查看答案和解析>>
科目:高中化学 来源: 题型:实验题
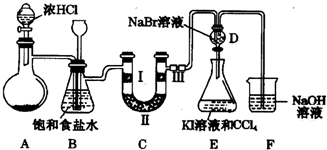
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
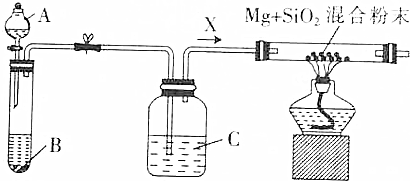
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在已知元素中具有最大的原子半径 | B. | 在空气中燃烧时生成氧化物Fr2O | ||
| C. | 氧化物对应的水化物是极强的碱 | D. | 其单质的熔点比金属钠的熔点低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加铁的量 | |
| B. | 将容器的体积缩小一半 | |
| C. | 压强不变,充入氮气使容器体积增大 | |
| D. | 加入催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com