
如图所示实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:
(1)在A试管内发生反应的化学方程式是_______________。
(2)B装置的作用是____________________________________________。
(3)在双球干燥管内发生反应的化学方程式为____________________________。
(4)双球干燥管内观察到的实验现象是__________________________________,上述实验现象说明____________________________________________________。
(5)若将干燥管内的Na2O2换成Na2O,则对于点燃的蚊香观察到的实验现象是______________________________。
(1)2NaHCO3△,Na2CO3+H2O+CO2↑ (2)吸收气体中的水蒸气(干燥CO2) (3)2Na2O2+2CO2===2Na2CO3+O2 (4)淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈 Na2O2能与CO2反应,生成白色粉末状物质和O2 (5)点燃的蚊香逐渐熄灭
解析 据实验装置图,可知实验步骤和顺序为:A中的NaHCO3受热分解产生的CO2和H2O(气)进入试管B,H2O(气)被浓硫酸吸收,从B中出来的CO2与C处Na2O2反应生成O2,从而促进蚊香的燃烧。第(5)问中,将Na2O2换成Na2O,则发生反应:Na2O+CO2===Na2CO3,无O2放出,所以蚊香会逐渐熄灭。


科目:高中化学 来源: 题型:
酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是
( )。
A.酯化反应的产物只有酯
B.酯化反应可看成取代反应的一种
C.酯化反应是有限度的
D.浓硫酸可作酯化反应的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
把铁片分别放入下列溶液中,铁片溶解,而溶液质量增加,但无气体产生,此溶液是( )
A.稀硫酸 B.AgNO3溶液 C.Fe2(SO4)3溶液 D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
等质量的CuO和MgO粉末分别在相同体积的硝酸中完全溶解,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol/L和b mol/L。则a与b的关系为( )
A.a=b B.a=2b C.2a=b D.a=5b
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种合成维生素的结构简式为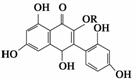 ,对该合成维生素的叙述正确的是( )
,对该合成维生素的叙述正确的是( )
A.该合成维生素有三个苯环
B.该合成维生素1 mol最多能中和5 mol氢氧化钠
C.该合成维生素1 mol最多能和含6 mol单质溴的溴水反应
D.该合成维生素可用有机溶剂萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
最近,国际上提出的“绿色化学”是指化学工业生产中
( )。
A.对废水、废气、废渣进行严格处理
B.化学生产中不排放任何有害物质
C.化工厂及周围种草、种树、种花,使工厂成为花园式工厂
D.以绿色植物为原料,以生物催化剂实现化工生产过程的化学
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是实验室干馏煤的装置图:
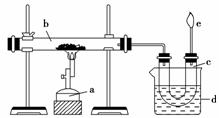
(1)指出图中仪器名称:a.________,d.________。
(2)仪器d的作用是________,c中液体有________和________,其中无机物里溶有________,可用________检验出来。有机物可以通过________的方法使其中的重要成分分离出来。
(3)e处点燃的气体主要成分有____________,火焰的颜色是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
为提高物质、能源利用率,化学工业近年提出共生工程,工业生产活动应尽可能多功能化。比如以硫酸工业的尾气、氨水、石灰石、焦炭、碳酸氢铵及氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
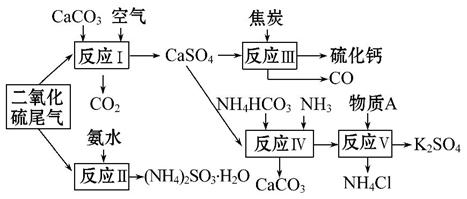
(1)除了可用于制备其他物质,SO2还可用于_________________;
(2)反应Ⅴ的原料A是________(填化学式);
(3)反应Ⅲ生成1 mol CaS转移的电子数为_________________________;
(4)生产中,向反应Ⅱ的溶液中加入适量还原性很强的对苯二酚等物质,其目的是________________________________________。
产物(NH4)2SO3可用于电厂等烟道气的脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式____________________________________;
(5)反应Ⅳ是往CaSO4悬浊液中加入碳酸氢铵、通入氨气,控制在60℃~70℃左右搅拌,温度太高和太低的不足分别是______________________________。
已知25℃时,Ksp(CaSO4)=7.10×10-5。向0.100 L含CaSO4固体的溶液中加入
2.22 g CaCl2粉末充分搅拌,假设溶液的体积变化忽略不计,所得溶液中c(S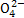 )=__________。
)=__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com