


科目:高中化学 来源: 题型:
 可逆反应A+aB?C+2D(a为化学计量数),已知B、C、D为气态物质.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )
可逆反应A+aB?C+2D(a为化学计量数),已知B、C、D为气态物质.反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示.下列说法不正确的是( )| A、T2>T1,p2>p1 |
| B、该反应为放热反应 |
| C、若a=2,则A为液态或固态物质 |
| D、恒温恒容,增加B的物质的量,B的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
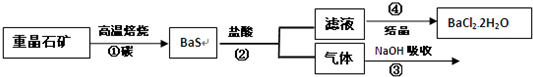
| c(Br-) |
| c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| △ |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中c(CO32-):c(HCO3-)<1:1 |
| B、溶液中c(OH-)+(CO32-)=c(H+)+c(HCO3-)+c(H2CO3) |
| C、向混合液中滴加少量稀盐酸或NaOH溶液,HCO3-的物质的量均会减少 |
| D、将混合液蒸干,水解加剧,最终得NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lg c(M),pCO32-=-lg c(CO32-).下列说法不正确的是( )
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=-lg c(M),pCO32-=-lg c(CO32-).下列说法不正确的是( )| A、MgCO3、CaCO3、MnCO3 的Ksp依次减小 |
| B、a 点可表示MnCO3 的饱和溶液,且c(Mn2+)=c(CO32-) |
| C、b 点可表示的CaCO3不饱和溶液,且c(Ca2+)<c(CO32-) |
| D、c 点可表示MgCO3 的不饱和溶液,且c(Mg2+)<c(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com