
| A. | 乙烯使酸性高锰酸钾溶液褪色 | B. | 乙烯使溴水褪色 | ||
| C. | 苯在铁粉存在下与液溴的反应 | D. | 苯的硝化反应 |
分析 有机物分子中的不饱和键断裂,断键原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应;有机物中的原子或原子团被其他的原子或原子团所代替生成新的化合物的反应叫取代反应,根据定义分析解答.
解答 解:A、乙烯使酸性高锰酸钾溶液褪色,是高锰酸钾和乙烯发生了氧化反应的结果,故A错误;
B、乙烯使溴水褪色,属于加成反应,故B正确;
C、苯在铁粉存在下与液溴的反应,生成溴苯,溴原子取代了苯环上的氢原子,属于取代反应,故C错误;
D、苯的硝化反,是硝基取代苯环上的氢原子,属于取代反应,故D错误;
故选B.
点评 本题主要考查了加成反应的判断,加成反应的条件是有机物中必须含有不饱和键(如碳碳双键、碳碳三键等).


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 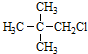 | B. | 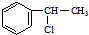 | C. | CH3Cl | D. | 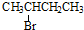 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
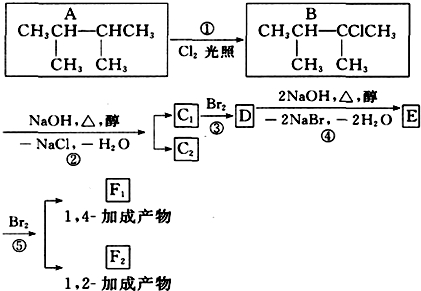
 .
. ;F 1的结构简式是
;F 1的结构简式是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:B>A,离子半径C<D | |
| B. | B的单质能与A的最高价氧化物发生置换反应 | |
| C. | 元素B和D能形成BD2型的共价化合物 | |
| D. | D的单质有毒,且干燥的单质D有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
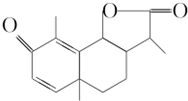 从菊科植物茼蒿的花中提取的一种有机化合物可用作驱肠虫剂,其结构简式如图所示.下列判断正确的是( )
从菊科植物茼蒿的花中提取的一种有机化合物可用作驱肠虫剂,其结构简式如图所示.下列判断正确的是( )| A. | 该有机化合物的分子式为C14H15O3 | B. | 该有机化合物含有两种官能团 | ||
| C. | 该有机化合物是芳香烃的衍生物 | D. | 该有机化合物可看作环状化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
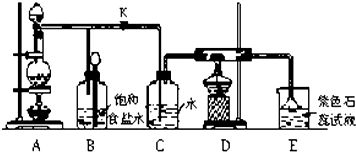
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
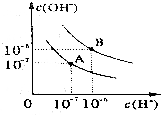 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com