
| 实验内容 | 实验现象 | 相关解释 | |
| A | 往Fe(OH)3胶体中逐滴滴入稀盐酸 | 先出现红褐色沉淀,后沉淀溶解 | 先胶体聚沉,后Fe(OH)3溶解 |
| B | NH3与Cl2混合 | 生成白烟 | NH3与Cl2发生化合反应生成NH4Cl |
| C | 等量的Cu分别与等体积足量的浓硝酸和稀硝酸反应 | 浓硝酸反应后呈绿色,稀硝酸反应后呈蓝色 | c(Cu2+)不同 |
| D | 加热硝酸铜固体,将带火星的木条伸入所得的气体中 | 生成红棕色气体,带火星木条复燃 | NO2有助燃性 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加盐酸,胶体先聚沉,后发生复分解反应;
B.反应生成氯化铵和氮气;
C.等量的Cu反应,均生成硝酸铜,且浓度相同;
D.生成红棕色气体为二氧化氮,N元素的化合价降低,O元素的化合价应升高,可知还生成氧气.
解答 解:A.往Fe(OH)3胶体中逐滴滴入稀盐酸,先发生聚沉现象生成氢氧化铁沉淀,会出现红褐色沉淀,后Fe(OH)3与HCl反应生成氯化铁和水,沉淀溶解,故A正确;
B.NH3与Cl2混合除了生成氯化铵,还会有氮气生成,不属于化合反应,故B错误;
C.将等质量的铜片分别与等体积、过量的浓硝酸和过量的稀硝酸反应后,所得溶液中Cu2+的浓度基本相等,颜色基本相同,不可能是c(Cu2+)浓度差异引起的,若溶液呈“绿色”可能是溶液中Cu2+与NO2共存的结果,故C错误;
D.加热发生2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑,二氧化氮的体积为氧气体积的4倍,生成红棕色气体为二氧化氮,带火星木条复燃说明氧气和NO2都有助燃性,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意使用的评价性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 稀硝酸中加入少量铁粉:Fe+2H++NO3-═Fe3++NO↑+H2O | |
| B. | 向NaHSO4溶液中滴加Ba(OH)2使溶液呈中性:SO42-+Ba2++2OH-+2H+═BaSO4↓+2H2O | |
| C. | FeI2溶液中加入少量的氯水:2Fe2++Cl2═2Fe3++2Cl- | |
| D. | 碳酸氢钠溶液加入少量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
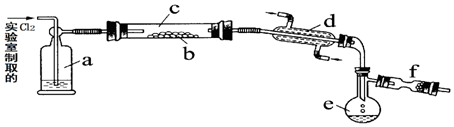
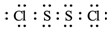 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C15H22O5 | B. | C15H20O5 | C. | C15H18O5 | D. | C15H24O5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO${\;}_{4}^{2-}$ | |
| B. | c(NaHCO3)=0.1 mol•L-1的溶液中:K+、C6H5O-、SO${\;}_{4}^{2-}$、CO32- | |
| C. | 含有大量Fe2+的溶液:Na+、SO42+、NH4+、Fe(CN)63? | |
| D. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、S2? |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
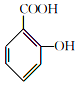 +
+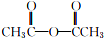 $→_{75-80℃}^{H_{3}PO_{4}}$
$→_{75-80℃}^{H_{3}PO_{4}}$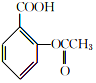 +CH3COOH
+CH3COOH| 名称 | 式量 | 性质 | 熔点/℃ | 沸点/℃ | 溶解度 | ||
| 水 | 乙醇 | 乙酸乙酯 | |||||
| 水杨酸 | 138 | 白色结晶粉末、无臭 | 157~159 | 211 | 溶 | 易溶 | 易溶 |
| 醋酸酐 | 102 | 无色液体、易燃、有醋酸味 | -73.1 | 138.6 | 易溶 | 溶 | 易溶 |
| 乙酸水杨酸 | 180 | 白色针状结晶 | 135 | 321.4 | 冰水微溶、热水可溶 | 易溶 | 微溶 |
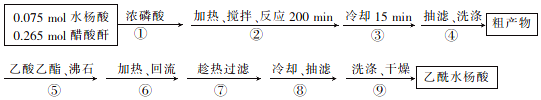
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
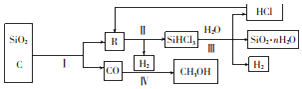
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原料来源广 | B. | 易燃烧,放出热量多 | ||
| C. | 产物无污染 | D. | 制取H2简单易行 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com