
某化学反应2A(g)⇌B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0.反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
实验
序号 时间
浓度
温度 0 10 20 30 40 50 60
1 800℃ 1.0 0.80 0.67 0.57 0.50 0.50 0.50
2 800℃ c2 0.60 0.50 0.50 0.50 0.50 0.50
3 800℃ c3 0.92 0.75 0.63 0.60 0.60 0.60
4 820℃ 1.0 0.40 0.25 0.20 0.20 0.20 0.20
根据上述数据,完成下列填空:
(1)在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为
(2)在实验2,A的初始浓度c2=1.0mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3>v1(填“<”、“=”或“>”),且c3 0mol/L(填“<”、“=”或“>”).
(4)比较实验4和实验1,可推测该反应是 (选填吸热、放热).理由是
考点: 化学平衡建立的过程.
专题: 化学平衡专题.
分析: (1)根据v=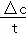 计算反应速率;
计算反应速率;
(2)比较实验1和实验2中平衡时的数据可得A的起始浓度,结合反应到达平衡的时间可知隐含的条件;
(3)根据浓度对反应速率的影响作判断;
(4)根据温度对平衡移动的影响判断.
解答: 解:(1)根据v=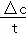 可计算出A的反应速率为
可计算出A的反应速率为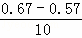 mol/(L•min)=0.01mol/(L•min),故答案为:0.01mol/(L•min);
mol/(L•min)=0.01mol/(L•min),故答案为:0.01mol/(L•min);
(2)比较实验1和实验2中平衡时的数据可知,平衡时A的浓度相等,温度也相同,所以起始浓度也相同,但实验2反应到达平衡的时间比实验1短,所以实验2中存在催化剂,故答案为:1.0;存在催化剂;
(3)比较实验1和实验3中的数据可知,在相同温度下,实验3中的A的平衡浓度大于实验1,所以反应过程中,反应速率也比实验1中的大,起始浓度也大于实验1中的,故答案为:>;>;
(4)比较实验4和实验1中数据可知,温度升高,起始浓度相同,但平衡A的浓度变小,说明平衡正向移动,故可判断该反应的正反应为吸反应,故答案为:吸热;升高温度,达平衡时A的浓度实验4较实验1小,说明平衡正向移动.
点评: 本题主要考查了化学反应速率的计算、影响化学反应速率和化学平衡的因素,中等难度,解题注意比较表中的数据从中获取信息.


科目:高中化学 来源: 题型:
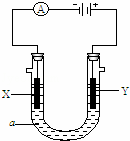
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式是 .在X极附近观察到的是 .
②Y电极上的电极反应式是 ,检验该电极反应产物的方法是 .
(2)如要用电解方法实现将铁片镀上一层金属铜,电解液a选用CuSO4溶液,则
①X电极的材料是Fe②Y电极反应式是 .
③已知开始时铁片与铜片的质量相同,当电路中有0.4摩尔电子通过时,两极质量相差 克.
查看答案和解析>>
科目:高中化学 来源: 题型:
可确认发生了化学平衡移动的是()
A. 化学反应速率发生了改变
B. 有气态物质参加的可逆反应达到平衡后,改变了压强
C. 由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变
D. 可逆反应达到平衡后,使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
把0.6molX气体和0.4molY气体混合于容积为2L的容器中,使其发生如下反应:3X(g)+Y(g)⇌nZ(g)+2W(g).5min末生成0.2molW,若测知以Z浓度变化表示的平均反应速率为0.01mol/L•min,则n的值为()
A. 4 B. 3 C. 2 D. 1
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 X(气)+Y(气)⇌2Z(气)+Q(Q>0),在一定条件下,反应物Y的转化率与反应时间(t)的关系如图所示.若使曲线a变为曲线b可采取的措施是()
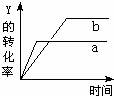
A. 加入催化剂 B. 降低温度 C. 增大压强 D. 增大Y的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下用NH3捕获CO2可以生成重要的有机化工产品﹣﹣三聚氰酸,反应的化学方程式如下:NH3+CO2→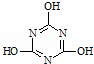 +H2O下列有关三聚氰酸的说法正确的是()
+H2O下列有关三聚氰酸的说法正确的是()
A. 分子式为C3H6N3O3
B. 分子中既含极性键,又含非极性键
C. 属于共价化合物
D. 生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图装置(夹持、加热装置已略)进行实验,由②中现象,不能证实①中反应发生的是
①中实验②中现象()
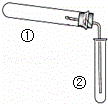
A. 铁粉与水蒸气加热 肥皂水冒泡
B. 加热NH4Cl和Ca(OH)2混合物 酚酞溶液变红
C. NaHCO3固体受热分解 澄清石灰水变浑浊
D. 石蜡油在碎瓷片上受热分解 Br2的CCl4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
多硫化钙[CaSx( x≤5)]、硫代硫酸钙组成的混合物称为石硫合剂,它是一种很好的植物杀虫剂,是由硫磺跟石灰、水等反应所得.不同比例的硫磺跟石灰在水溶液中反应,可生成不同的多硫化钙与硫代硫酸钙.
3Ca(OH)2+8S 2CaS3+CaS2O3+3H2O;3Ca(OH)2+6S
2CaS3+CaS2O3+3H2O;3Ca(OH)2+6S 2CaS2+CaS2O3+3H2O
2CaS2+CaS2O3+3H2O
完成下列计算:
(1)硫磺溶解在硫化钠溶液中生成一种多硫化物,该多硫化物中硫元素的质量分数为0.736,则该Na2Sx中x=4.
(2)取某石硫合剂(假如只含两种含硫化合物)250mL(密度为1.12g/cm3)通入足量CO2使其快速分解.原理如下:Sx2﹣+2H2O+2CO2→(x﹣1)S↓+H2S↑+2HCO3﹣;S2O32﹣+H2O+CO2→HSO3﹣+HCO3﹣+S↓
完全反应后共收集到气体1.12升(标准状况)(忽略气体在溶液中的溶解),则该石硫合剂中多硫化钙的物质的量浓度为 ;硫代硫酸钙的质量分数为 .(答案用小数表示,保留2位有效数字)
(3)如果把生石灰、硫磺和水按质量比7:16:70的配比完全反应后,只生成两种含硫的化合物,则该石硫合剂中多硫化钙与硫代硫酸钙的物质的量之比是 ;多硫化钙的化学式是 .
(4)现有生石灰50.4g、硫磺96g、水504g恰好完全反应生成三种多硫化钙,除生成CaS4之外还有二种多硫化钙.请推算这二种多硫化钙可能的物质的量之比 (写出推理过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
化学实验要注意安全,下列行为符合安全要求的是( )
|
| A. | 汽油着火时,立即用水灭火 |
|
| B. | 稀释浓硫酸时,将水倒入浓硫酸中 |
|
| C. | 浓NaOH溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 |
|
| D. | 浓硫酸溅到皮肤上,立即用稀NaOH溶液洗涤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com