
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJmol﹣1 , 甲醚可作燃料电池的燃料.
(1)写出甲醚燃烧的热化学方程式;已知H2(g)和C(s)的燃烧热分别是285.8kJmol﹣1、393.5kJmol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H=kJmol﹣1;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是(选填编号,注意大小写).
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将(填“变大”、“变小”或“不变”,下同).
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池的负极反应式的其中一个产物是CO32﹣ , 请写出该反应的负极反应式;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500mL NaCl溶液,装置如图所示,请写出电解过程中Y电极附近观察到的现象是;当燃料电池消耗2.8LO2(标准状况下)时,计算此时:NaCl溶液中C(OH﹣)=mol/L(假设溶液的体积不变,气体全部从溶液中逸出). 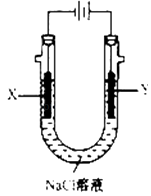
【答案】
(1)CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;﹣378.8
(2)ad;变小
(3)CH3OCH3+16OH﹣﹣12e﹣=2CO32﹣+11H2O
(4)Y电极附近溶液中有气体产生,上部分呈黄绿色;1
【解析】解:(1)甲醚的燃烧热为1455kJ/mol,则燃烧方式的热化学方程式为:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;
H2(g)和C(s)的燃烧热分别是285.8kJmol﹣1、393.5kJmol﹣1 , 热化学方程式为
①H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.8KJ/mol;
O2(g)=H2O(l)△H=﹣285.8KJ/mol;
②C(s)+O2(g)=CO2(g)△H=﹣393.5KJ/mol;
③CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;
依据盖斯定律计算①×3+②×2﹣③得到反应热化学方程式为:2C(s)+3H2(g)+ ![]() O2(g)═CH2OCH3(g)△H=﹣169.4kJ/mol;即可得到4C(s)+6H2(g)+O2(g)═2CH2OCH3(g)△H=﹣378.8kJ/mol;
O2(g)═CH2OCH3(g)△H=﹣169.4kJ/mol;即可得到4C(s)+6H2(g)+O2(g)═2CH2OCH3(g)△H=﹣378.8kJ/mol;
所以答案是:CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H1=﹣1455kJ/mol;﹣378.8kJ/mol;(2)①a、在反应达平衡前,c(H2)与c(H2O)的比值在变小,故当c(H2)与c(H2O)的比值保持不变时,反应达平衡,故A选;
b、单位时间内有2mol H2消耗时一定会有1mol H2O生成,故不能作为平衡的标志,故B不选;
c、本反应的反应物和生成物全是气体,根据质量守恒可知,在反应过程中气体的质量一直不变,而又是恒容的容器,即气体体积不变,故气体密度ρ= ![]() 一直不变,故密度不变不能作为平衡的标志,故c不选;
一直不变,故密度不变不能作为平衡的标志,故c不选;
d、此反应是个气体的物质的量有改变的反应,即在平衡之前,容器中气体的物质的量和压强在变化,故当压强不变时,说明反应达平衡,故d选.
所以答案是:ad;②反应为放热反应,故升高温度,平衡左移,达到新的平衡,CH3OCH3的产率将变小;
所以答案是:变小;(3)原电池负极发生氧化反应,甲醚在负极放电,碱性条件下生成碳酸根与水,电极反应式为:CH3OCH3+16OH﹣﹣12e﹣=2CO32﹣+11H2O;
所以答案是:CH3OCH3+16OH﹣12e﹣=2CO2﹣3+11H2O;(4)电解池中Y电极为阳极,溶液中氯离子失电子发生氧化反应生成氯气,现象是冒气泡,上部溶液呈黄绿色;
当燃料电池消耗2.8LO2(标准状况下)物质的量= ![]() =0.125mol,电极反应为O2+2H2O+4e﹣=4OH﹣ , 电子转移为0.5mol,阴极电极方程式:2H2O+2e﹣=2 OH﹣+H2 , 所以n(OH﹣)=0.5 mol,c(OH﹣)=
=0.125mol,电极反应为O2+2H2O+4e﹣=4OH﹣ , 电子转移为0.5mol,阴极电极方程式:2H2O+2e﹣=2 OH﹣+H2 , 所以n(OH﹣)=0.5 mol,c(OH﹣)= ![]() =1 mol/L;
=1 mol/L;
所以答案是:Y电极附近溶液中有气体产生,上部分呈黄绿色;1.
【考点精析】通过灵活运用化学平衡状态的判断,掌握状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等即可以解答此题.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】固定容积为2L的密闭容器中发生反应xA(g)+yB(g)zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系.结合图象判断,下列结论正确的是( ) 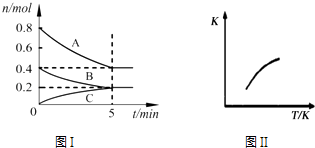
A.该反应可表示为:2A(g)+B(g)C(g)△H<0
B.t℃时该反应的平衡常数K=6.25
C.当容器中气体密度不再变化时,该反应达到平衡状态
D.t℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述中正确的是( )
A. 金属钠可以保存在少量水中 B. 金属钠是银白色, 但露置于空气中会变暗
C. 钠在空气中燃烧生成白色的 Na2O D. 钠投入CuSO4溶液中可观察到有红色物质析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( ) 
A.草酸二酯的分子式为C26H24Cl6O8
B.1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH
C.该有机物能发生加成反应、取代反应、氧化反应
D.1 mol草酸二酯与氢气完全反应,需要氢气6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11)。该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如下图所示(注意图中的反应式不完整)。
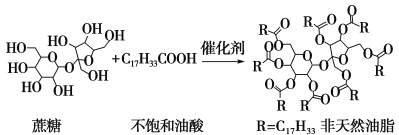
下列说法正确的是( )
A.蔗糖酯也是高级脂肪酸的甘油酯,属于油脂类物质
B.该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应
C.非天然油脂为高分子化合物
D.该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是 ( )
A. H+、Ca2+、Cl-、CO32-B. Na+、Fe3+、OH-、SO42-
C. K+、Na+、OH-、Cl-D. Cu2+、Ba2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.含氧酸能起氧化作用,无氧酸则不能
B.阳离子只有氧化性,阴离子只有还原性
C.失电子难的原子获得电子的能力一定强
D.化学反应中,某元素由化合态变成游离态,此元素可能被氧化,也可能被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,工作原理如图所示.下列有关说法错误的是( ) 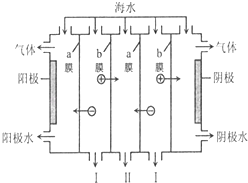
A.阳极可发生电极反应:2Cl﹣﹣2e﹣═Cl2↑
B.阴极附近溶液的pH减小
C.a膜为阴离子交换膜,b膜为阳离子交换膜
D.I,II分别是淡水、浓海水出口
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com