
下列说法错 误的是
误的是
A.58.5g NaCl溶于1L水中配得1mol/L NaCl溶液
B.在标准状况下,44.8LHCl气体溶于水配成1L溶液,所得溶 液中溶质的物质的量浓度为2mol/L。
液中溶质的物质的量浓度为2mol/L。
C.在标准状况下,22.4L氨气溶于水配成1L溶液,从所得溶液中取出10mL,其物质的量浓度为1mol/L。
D.1mol/L的CaCl2溶液1L,取出100mL,含0.2molCl-。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 称取12.5g胆矾配成500mL溶液 | B. | 称取8.0g胆矾配成500mL溶液 | ||
| C. | 称取8.0g硫酸铜,加入500mL水 | D. | 称取7.68g硫酸铜,加入500mL水 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
(1)可逆反应2Cl2(g)+2H2O(g  4HCl(g)+O2(g) (△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
4HCl(g)+O2(g) (△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
①降低温度,Cl2的转化率___ _______;υ(逆)______________;
②保持容器体积不变,加入He,则HCl的物质的量__________。
③保持容器压强不变,加入He,则O2的物质的量__________;
④若温度和体积不变,反应从Cl2和H2O开始至平衡,在这个变化过程中,容器内气体的密度 ____,相对分子质量_________。
(2)氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+ 6C(s) + 2N2(g) Si3N4(s)+ 6CO(g)
Si3N4(s)+ 6CO(g)
①该反应的平衡常数表达式为 K= ;
②若知上述反应为吸热反应,升高温度,其平衡常数值 (填“增大”、“减小”或“不变”);若已知CO生 成速率为υ(CO)=18mol·L-1·min-1,则N2消耗速率为υ(N2)= 。
成速率为υ(CO)=18mol·L-1·min-1,则N2消耗速率为υ(N2)= 。
③达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率υ与时间t的关系如下图。图中t4时引起平衡移动的条件可能是 ;图中表示平衡混合物中CO的含量最高的一段时间是 。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
已知:(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H1
(2)C(s)+O2(g)=CO2(g)△H2
(3)2H2(g)+O2(g)=2H2O(l)△H3
(4)2CO2(g)+4H2(g)=CH3COOH(l)+2H2O(l)△H4
(5)2C(s)+2H2(g)+O2(g)=CH3COOH(l)△H5
下列关于上述反应的焓变的判断正确的是( )
A.△H1>0,△H2<0 B.△H5=2△H2+△H3﹣△H1
C.△H3>0,△H5<0 D.△H4=△H1﹣2△H3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上教学质检化学试卷(解析版) 题型:填空题
将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为_______________。
(2)该溶液中NaOH的质量分数为__________
(3)从该溶液中取出10 mL,其中NaOH的物质的量浓度为__________,NaOH的质量分数为__________,溶液的密度为___________,含NaOH的质量为_________,含NaOH的物质的量为__________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为_________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上教学质检化学试卷(解析版) 题型:选择题
下列各组物质中,所含分子数相同的是
A.10g H2和10g O 2 B.5.6LCCl4(标准状况)和11gCO2
2 B.5.6LCCl4(标准状况)和11gCO2
C.9gH2O和0.5molBr2 D.224mL H2(标准状况)和0.1molN2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上教学质检化学试卷(解析版) 题型:填空题
砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等,氮、磷、砷位于同一主族,回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga As,第一电离能Ga As。(填“大于”或“小于”)
(3)氮原子的L层中有__________对成对电子,NH4+的立体构型是__________,其中心原子的杂化方式为__________;PCl3属于含有 键的 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西藏民族学院附中高二上月考二化学卷(解析版) 题型:填空题
研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
Ⅰ.(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:
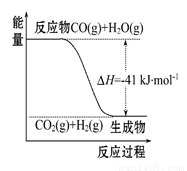
①反应的热化学方程式为 。
②已知:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131 kJ·mol-1,
则C(s)+CO2(g)=2CO(g) ΔH= 。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;N—H键的键能是391
mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ·mol-1,H—H键的键能是436.0 kJ·mol-1;N—H键的键能是391 .55 kJ·mol-1。则N
.55 kJ·mol-1。则N 2(g)+3H2(g)=2NH3(g) ΔH= 。
2(g)+3H2(g)=2NH3(g) ΔH= 。
Ⅱ.下图是一个化学过程的示意图,回答下列问题:

(1)甲池是 装置,乙装置中电极A的名称 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中电极B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式)。
(3)一段时间,当丙池中产生112 mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃时的pH= 。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应可区分胶体和溶液 | |
| B. | 煤可经分馏获得洁净的燃料 | |
| C. | 非金属材料中不可以含有金属元素 | |
| D. | 电解氯化镁饱和溶液,可制得金属镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com