
A.左边注射器内的活塞高度比右边注射器内的活塞高度要高?
B.左边注射器内的活塞与右边注射器内的活塞移动的方向和高度都相同?
C.左边烧瓶内的颜色比右边烧瓶内的颜色深?
D.两烧瓶内的化学平衡都发生了移动
科目:高中化学 来源:2006年五月理科综合模拟化学部分、(第一套) 题型:022
| |||||||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
测定乙醇分子结构是经典的定量实验之一,反应原理为乙醇+钠(足量)→乙醇钠+氢气。选用如下图所示仪器和导管组装实验装置。
| 1 | 2 | 3 | 4 | ||
|
|
|
|
| ||
| 每个橡皮塞上都打了两个孔 | |||||
| 5 | 6 | 7 | |||
|
|
|
| |||
| 每个橡皮塞上都打了两个孔 | |||||
(1)气体发生器置于左侧,气体向右方流动,所用仪器与导管依次连接序号为:6接____________接____________接____________接____________接____________。
(2)进行实验时的操作如下(每项进行一次)
①从分液漏斗中逐滴把无水酒精加入烧瓶中,并控制反应速率,酒精加完后再关闭活塞
②在广口瓶中注入适量的水
③待烧瓶冷却至室温后对量筒读数
④把定量的V mL酒精无损的倒入分液漏斗中
⑤检查装置的气密性
⑥预先将钠块在二甲苯中熔化成小钠珠,冷却后倒入烧瓶中,塞紧橡皮塞
⑦估计反应接近完成,用酒精灯对烧瓶微热,使反应完成,再撤掉酒精灯
正确的操作序号为____________。
(3)将小钠块制成小珠的目的是________________________________________________。
(4)如果此实验的数据视作标准状况下的数据,无水乙醇的密度为ρ g·cm-3,V mL乙醇完全反应后,量筒内的液面读数为m mL,则乙醇分子中能被取代的氢原子数是____________。
(5)某学生认为实验成功的关键有:①装置的气密性要好;②实验开始前准确确定乙醇的量;③钠足量;④广口瓶中必须充满水;⑤氢气体积的测算方法正确、数值准确。其中必要的为____________________________________。
(6)读数时,量筒内的液面高于广口瓶中的液面会使测得结果____________(偏低、偏高、不影响)
查看答案和解析>>
科目:高中化学 来源: 题型:
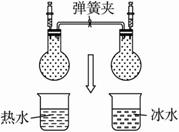
如下图所示25℃时,在烧杯A中装有50.0 mL水,烧杯B中装有0.50 mol?L-1盐酸50.0 mL,把NO2和N2O4的混和气体盛在两个连通的烧瓶C、D里,然后用夹子夹住橡皮管,把C烧瓶放人A烧杯中,D烧瓶放人B烧瓶中。往A烧杯中加入50.0 g NH4NO3粉末搅拌使其完全溶解,往B烧杯中加入2.0g NaOH固体搅拌并使其溶解后。回答下列问题:

![]()
(1) 烧杯B中温度(填“升高”、“降低”或“不变”)__________。
![]() (2)已知在NO2生成N2O4的可逆反应: 2NO2(g)
(2)已知在NO2生成N2O4的可逆反应: 2NO2(g) ![]() N2O4(g) △H<O,从上面实验可知C烧瓶内混和气体颜色(填“变浅”、“变深”或“不变”)______;
N2O4(g) △H<O,从上面实验可知C烧瓶内混和气体颜色(填“变浅”、“变深”或“不变”)______;
![]() (3)若实验测得B烧杯中酸碱中和反应放热1.4325 kJ,则NaOH溶液和HCl溶液发生中和反应的热化学方程式为___________。
(3)若实验测得B烧杯中酸碱中和反应放热1.4325 kJ,则NaOH溶液和HCl溶液发生中和反应的热化学方程式为___________。
![]() (4)若起始时在D烧瓶中充人m g N2O4,此时测得烧瓶中压强为1.01×105Pa,当可逆反应:N2O4(g)
(4)若起始时在D烧瓶中充人m g N2O4,此时测得烧瓶中压强为1.01×105Pa,当可逆反应:N2O4(g) ![]() 2NO2达到化学平衡状态时压强变为1.515×105Pa,则平衡混和气体的平均相对分子质量为:__________________。(精确到小数点后两位)
2NO2达到化学平衡状态时压强变为1.515×105Pa,则平衡混和气体的平均相对分子质量为:__________________。(精确到小数点后两位)
![]()
![]()
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组用模拟制备氨基甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g)
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组用模拟制备氨基甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g) ![]() NH2COONH4(s) ΔH<0
NH2COONH4(s) ΔH<0
(1)如用右图装置制取氨气,选择的试剂可以是(填序号)
A.氯化铵固体与消石灰固体 B.浓氨水与碱石灰
C.浓氨水与NaOH固体 D.氯化铵溶液与烧碱溶液
(2)制备氨基甲酸铵的装置如下图,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。 当悬浮物较多时,停止制备。(注:四氯化碳与液体石蜡均为惰性介质)
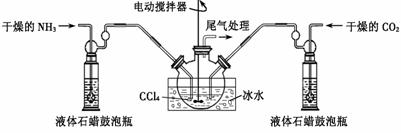
 ①发生器用冰水冷却的原因是________ __ _;液体石蜡鼓泡瓶的作用是______________________________ __。
①发生器用冰水冷却的原因是________ __ _;液体石蜡鼓泡瓶的作用是______________________________ __。
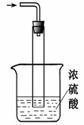
②尾气处理装置如右图所示。
双通玻璃管的作用: ;
浓硫酸的作用: 、________ _。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820 g,用足量石灰水充分处理后,使所有碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000 g。则样品中氨基甲酸铵的物质的量分数为____________。
[Mr(NH2COONH4)=78、Mr(NH4HCO3) =79、Mr(CaCO3)=100]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com