
【题目】某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为______________,名称为____________________。
(2)A中的碳原子是否都处于同一平面?________(填“是”或“不是”);A分子是否存在顺反异构体________(填“是”或“否”)。
(3)已知A、B、C有如下转化关系:
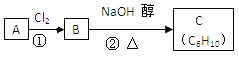
则反应②的化学方程式为____________;反应的类型是_____________
【答案】![]() 2,3—二甲基—2—丁烯 是 否
2,3—二甲基—2—丁烯 是 否 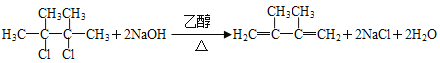 消去反应
消去反应
【解析】
(1)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,又因为核磁共振氢谱表明分子中只有一种类型的氢,其结构简式应为![]() ;
;
(2)根据乙烯结构,结合顺反异构的特点判断;
(3)由A可知B为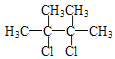 ,B在NaOH醇溶液中发生消去反应,根据C的分子式可知C为
,B在NaOH醇溶液中发生消去反应,根据C的分子式可知C为![]() ,以此可写出反应的方程式。
,以此可写出反应的方程式。
(1)A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,则A应为烯烃,设分子式为CnH2n,则有14n=84,n=6,又因为核磁共振氢谱表明分子中只有一种类型的氢,其结构简式应为![]() ,名称为2,3—二甲基—2—丁烯;
,名称为2,3—二甲基—2—丁烯;
(2)由于碳碳双键是平面型结构,而4个甲基中碳原子与碳碳双键的碳原子直接相连,所以6个碳原子处于同一平面上,因碳碳双键中每个C连接烃基相同,则不存在顺反异构;
(3)由A与Cl2发生加成反应生成的B为 ,B在NaOH醇溶液中发生消去反应,根据C的分子式可知C为
,B在NaOH醇溶液中发生消去反应,根据C的分子式可知C为![]() ,则反应的方程式为
,则反应的方程式为 。
。


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。
Ⅰ.实验室制备Cl2的离子方程式____________________________。
Ⅱ.某兴趣小组通过下图装置(夹持装置略)ClO2对制备、吸收、释放和应用进行了研究。
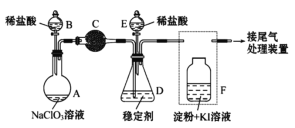
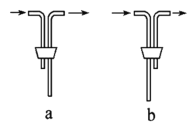
(1)仪器B的名称是___________。安装F中导管时,应选用上图中的_________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2 在D中被稳定剂充分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是___________ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________________,装置F中的现象是________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述错误的是
A. 0.5mol/LCuCl2溶液中含有的Cl-数目为NA
B. 42gC2H4和C4H8的混合气中含有氢原子数为6NA
C. 标准状况下,H2和CO混合气体4.48L在足量O2中充分燃烧消耗O2分子数为0.1NA
D. 在反应4Cl2+8NaOH=6NaCl+NaClO+NaClO3+4H2O中,消耗1molCl2时转移的电子总数为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷及其化合物被运用在农药、除草剂、杀虫剂与多种合金中,其中三氧化二砷(AS2O3)被称为砒霜,是一 种毒性很强的物质。回答下列问题:
(1)As在元素周期表中的位置是_____________,AsH3的电子式_________。
(2)一定条件下,雄黄(As4S4)与As2O3的转化关系如图所示。若该反应中1mol As4S4(其中As元素的化合价为+2)参加反应时,转移28mole-,则物质a为_________(填化学式)。

(3)焦炭真空冶炼砷时需加入催化剂,其中部分反应的热化学方程式如下:
反应 I .As2O3(g) +3C(s) ![]() 2As(g) +3CO(g)
2As(g) +3CO(g) ![]() =a kJ· mol-1
=a kJ· mol-1
反应 II.As2O3(g) +3C(s) ![]()
![]() As4(g) +3CO(g)
As4(g) +3CO(g) ![]() =b kJ ·mol-1
=b kJ ·mol-1
反应III.As4(g) ![]() 4As(g)
4As(g) ![]()
① ![]() =_________kJ ·mol-1 (用含a,b的代数式表示)。
=_________kJ ·mol-1 (用含a,b的代数式表示)。
②反应中催化剂的活性会因为反应II[生成As4(g)]的发生而降低,同时存在的反应III可使As4(g)的量减少。已知催化剂X、Y的相关数据如表所示:
反应II | 反应III | ||
活化能/ (kJ ·mol -1 ) | 催化剂X | 56 | 75 |
催化剂Y | 37 | 97 | |
由表中数据判断催化剂X_______ (填“优于”或“劣于”)催化剂Y。
(4)298 K 时,将 20mL 3xmol·L-1 Na3AsO3溶液、20 ml 3xmol·L-l I2溶液和 20mL 6xmol· L-l NaOH 溶液混合(忽略溶液体积变化),发生反应:![]() (aq) +I2(aq) +2OH-(aq)
(aq) +I2(aq) +2OH-(aq)![]()
![]() (aq) +2I-(aq) +H2O(l)。溶液中 c(
(aq) +2I-(aq) +H2O(l)。溶液中 c(![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
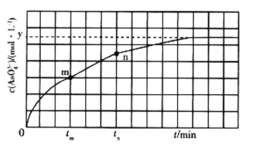
①下列可说明反应达到平衡的是_______ (填标号)。
a.v(I- ) =2v(![]() )
)
b.溶液的c(OH-)不再发生变化
c.c(I-) =ymol· L-1
d.c(![]() )/c(
)/c(![]() )不再发生变化
)不再发生变化
e.c(Na+) =5xmol· L-1
②tm min时,v正(![]() )_______ (填“大于”“小于”或“等于”)v逆(
)_______ (填“大于”“小于”或“等于”)v逆( ![]() )。
)。
③tm min时v逆( ![]() ) _______ (填“大于”“小于”或“等于”)tn时v逆(
) _______ (填“大于”“小于”或“等于”)tn时v逆( ![]() ),理由是___________________。
),理由是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu组成的原电池示意图,某小组做完该实验后,在读书卡片上记录如下,卡片上描述合理的是( )
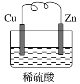
实验记录:
①导线中电流方向:Zn→Cu
②Cu极上有气泡产生,发生还原反应
③锌片变薄
实验结论:
④Zn为正极,Cu为负极
⑤正极反应式:Cu-2e-=Cu2+,发生氧化反应
⑥H+向Cu极移动,SO42-向Zn极移动
A.②③⑥B.④⑤⑥
C.③④⑤D.①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
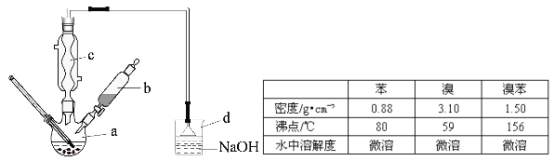
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)利用反应CuSO4+Fe===Cu+FeSO4可设计为原电池。
(1)负极材料是________(写名称),电极反应为__________________________________。
(2)正极电极反应式为______________________。
(3)溶液中SO42-向________极移动。
(II)工业合成氨反应:N2+3H2![]() 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。
(4)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总理论数值,其原因是____________________________。
(5)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为________mol·L-1·min-1。
(6)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是________。
a.正反应速率和逆反应速率相等 b.正反应速率最大,逆反应速率为0
c.反应达到最大限度 d.N2和H2的浓度相等
e.生成1 mol N2的同时,消耗2 mol NH3 f.生成3 mol H2的同时,生成2 mol NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸氯丙嗪是一种多巴胺受体的阻断剂,临床有多种用途。化合物Ⅲ是盐酸氯丙嗪制备的原料,可由化合物I和Ⅱ在铜作催化剂条件下反应制得。
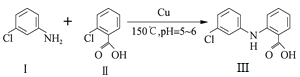
(1) Cu基态核外电子排布式为________________。
(2) 1 mol化合物Ⅰ分子中含有σ键数目为________。
(3) 化合物Ⅲ分子中sp3方式杂化的原子数目是____________。
(4) 向[Cu(NH3)4]SO4溶液中通入SO2至微酸性,有白色沉淀生成。分析表明该白色沉淀中Cu、S、N的物质的量之比为1∶1∶1,沉淀中有一种三角锥形的阴离子和一种正四面体形的阳离子。
①[Cu(NH3)4]SO4中存在的化学键类型有________(填字母)。
A.共价键 B.氢键 C.离子键 D.配位键 E. 分子间作用力
② 铜的氢化物的晶体结构如图所示,写出该晶体的化学式:____________。
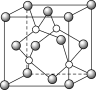
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用18mol/L 浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 溶解
④ 转移、洗涤 ⑤ 定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是 mL ,量取浓硫酸所用的量筒的规格是 。
(从下列中选用 A. 10mL B. 25mL C. 50mL D. 100ml)
(2)第③步实验的操作是
。
(3)第⑤步实验的操作是
。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A. 所用的浓硫酸长时间放置在密封不好的容器中
B. 容量瓶用蒸馏水洗涤后残留有少量的水
C. 所用过的烧杯、玻璃棒未洗涤
D. 定容时俯视溶液的液凹面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com