
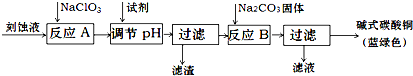
| ���� | Cu��OH��2 | Fe ��OH��2 | Fe ��OH��3 |
| ��ʼ����pH | 4.2 | 5.8 | 1.2 |
| ��ȫ����pH | 6.7 | 8.3 | 3.2 |
���� �������̿�֪����Һ�м���������ƽ��������������������ӣ�Ȼ����������ͭ��̼��ͭ������Һ��pH��������������ȥ�����ӣ����˺����̼������Һ���ɼ�ʽ̼��ͭ�����˺�õ���ʽ̼��ͭ��
��1���������Ӳ����׳�ȥ����Ҫ����������ƽ��������������������ӣ����ڳ�ȥ���ʣ�
��2������PHʹ�������ӳ�����ȫ����ͭ���Ӳ��ܿ�ʼ������Ϊ�˲��������ʣ�����ʵļ���������̼��ͭ��
��3����ӦB���¶�����ߣ�̼��ͭ������ͭ���ȷֽ�Ϊ����ͭ��
��4��ȡ���һ��ϴ��Һ���ʵ���������ữ����������Һ�����Ƿ�����������Ƽ��飻
��5����Cu2+��CO32-����CuCO3������
��Cu2+��CO32-��ˮ��Ӧ����Cu��OH��2�����Ͷ�����̼��
��������Cu��OH��2��CuCO3�Ļ�������ɼ�ʽ�Σ�˵�������ܽ�������
��6����Ʒ������������Ƴ�����aCuCO3•bCu��OH��2•cH2O�����������֣�֪�����������ֵ����ݣ���һ���ֵ����ݿ�����Ʒ����������֪�����ֵ�������ã�
��� �⣺�������̿�֪���Ʊ���ʽ̼��ͭ�ķ���Ϊ����Һ�м���������ƽ��������������������ӣ�Ȼ����������ͭ��̼��ͭ������Һ��pH��������������ȥ�����ӣ����˺����̼������Һ���ɼ�ʽ̼��ͭ�����˺�õ���ʽ̼��ͭ��
��1�����ڳ���������������pH���ڳ�������������pH������Ӧ�ð����������������������ӣ�Ȼ���ٳ��������������Ƶ������ǽ�Fe2+������Fe3+��
����Ϊ��������ȫ�����õ�����������������
�ʴ�Ϊ����Fe2+������Fe3+�����ճ�ȥ��Fe��OH��3��
��2������pHʹ�������ӳ�����ȫ����ͭ���Ӳ��ܿ�ʼ���������ڷ�ӦA����Һ��pH��ΧӦΪ3.2-4.2����ˮ�������ƾ������������ӣ����������ʹpH���ߣ�Ϊ�˲��������ʣ�����ʵļ���������̼��ͭ��
�ʴ�Ϊ��3.2-4.2��d��
��3����ӦB���¶�����ߣ�̼��ͭ������ͭ�������ȷֽ���������ͭ��
�ʴ�Ϊ��CuO��
��4�������˵õ��IJ�Ʒϴ��ʱ���жϲ�Ʒ�Ѿ�ϴ���ķ����Ͳ���Ϊ��ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ�������������Ҳ���֣�
��5���ٽ�Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ�������Cu2+��CO32-����CuCO3���������ӷ���ʽΪ��Cu2++CO32-=CuCO3����
�ʴ�Ϊ��Cu2++CO32-=CuCO3����
��Cu2+��CO32-��ˮ����˫ˮ�ⷴӦ����Cu��OH��2�����Ͷ�����̼�����ӷ���ʽΪ��Cu2++CO32-+H2O=Cu��OH��2��+CO2����
�ʴ�Ϊ��Cu2++CO32-+H2O=Cu��OH��2��+CO2����
��������Cu��OH��2��CuCO3�Ļ�������ɼ�ʽ�Σ�˵�������ܽ�������������������ͭҲ����̼��ͭ��
�ʴ�Ϊ��̼��ͭ��������ͭ���ܽ�������
��6����ʽ̼��ͭ����ɿɱ�ʾΪ��aCuCO3•bCu��OH��2•cH2O���ֽ��������������ɣ�������̼��CuO��ˮ��Ҫ�ⶨ����ɣ��ٳ�����Ʒ����������֪�����۲��CO2�������ܲ��ˮ�����������ݳ���CuO��������������֪�����е������������ɣ���һ���ֵ����ݿ�����Ʒ����������֪�����ֵ�������ã�
�ʴ�Ϊ���ٳ�����Ʒ����������֪�����۲��CO2�������ܲ��ˮ�����������ݳ���CuO��������������֪�����е������������ɣ���һ���ֵ����ݿ�����Ʒ����������֪�����ֵ�������ã�
���� ���⿼����ʵ��̽�����ʷ��뷽�����������ʵķ����жϣ��漰���ӷ�Ӧ�϶࣬�������������ǹؼ�����Ŀ�Ѷ��еȣ�


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | X | Y | 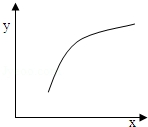 |
| A | �¶� | �����ڻ��������ܶ� | |
| B | A�����ʵ��� | B��ת���� | |
| C | ���������� | C��������� | |
| D | ����Ar�����ʵ��� | �淴Ӧ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʵ�鲻��Ҫָʾ�� | |
| B�� | ����Ͳ��ȡ������������ | |
| C�� | H2SO4��Ũ��Ϊ1.00 mol•L-1 | |
| D�� | �μӷ�Ӧ��H+��OH-�����ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��ȼ����С��110.5 kJ/mol | |
| B�� | �ٵķ�Ӧ��Ϊ221 kJ/mol | |
| C�� | Ũ������ϡNaOH��Һ��Ӧ���к���Ϊ-57.3 kJ/mol | |
| D�� | ϡ������ϡNaOH��Һ��Ӧ����1 molˮ���ų�������С��57.3 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ������������������ֱ���ȫȼ�գ����߷ų������� | |
| B�� | ��H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ•mol-1��֪��������5mol H2SO4��Ũ�����뺬1mol NaOH��ϡ��Һ��ϣ��ų�����������57.3kJ | |
| C�� | ��C��ʯī��=C�����ʯ����H=+1.90kJ•mol-1��֪�����ʯ��ʯī�ȶ� | |
| D�� | ��101kPaʱ��2g H2��ȫȼ������Һ̬ˮ���ų�285.8kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ�� 2H2��g��+O2��g��=2H2O��l����H=-285.8kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H5OH��l��+3O2��g���T2CO2��g��+3H2O��g����H=-1367.0 kJ•mol-1��ȼ���ȣ� | |
| B�� | NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=+57.3 kJ•mol-1���к��ȣ� | |
| C�� | S��s��+O2��g���TSO2��g����H=-269.8 kJ•mol-1����Ӧ�ȣ� | |
| D�� | 2H2��g��+O2��g���T2H2O��l����H=571.6kJ•mol-1����Ӧ�ȣ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 436 kJ | B�� | 557 kJ | C�� | 920 kJ | D�� | 618 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����һ���ǻ����� | B�� | ����ʿ����ǻ���� | ||
| C�� | ����ʲ�һ���ǻ����� | D�� | �����һ���ǵ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com