
分析 (1)NaOH溶液中c(OH-)=0.5mol/L×0.06L=0.03mol,硫酸中c(H+)=0.4mol/L×0.04L×2=0.032mol>0.03mol,所以混合溶液呈酸性,混合溶液中c(H+)=$\frac{0.032mol-0.03mol}{(0.06+0.04)L}$=0.2mol/L,pH=-lgc(H+);
(2)n[Ba(OH)2]=$\frac{2.1375g}{171g/mol}$=0.0125mol,n(BaSO4)=$\frac{1.165g}{233g/mol}$=0.005mol,根据S原子守恒得n(H2SO4)=n(BaSO4)=0.005mol,硫酸中n(H+)=2n(H2SO4)=2×0.005mol=0.01mol,
反应后溶液中pH=13,则溶液中c(OH-)=0.1mol/L,设盐酸中n(H+)为xmol,则$\frac{0.0125mol×2-0.01mol-xmol}{0.05L}$=0.1mol/L,x=0.01,
根据Cl、H原子守恒得n(Cl-)=n(HCl)=n(H+) (盐酸)=0.01mol,再根据c=$\frac{n}{V}$计算氯离子、硫酸根离子浓度.
解答 解:(1)NaOH溶液中c(OH-)=0.5mol/L×0.06L=0.03mol,硫酸中c(H+)=0.4mol/L×0.04L×2=0.032mol>0.03mol,所以混合溶液呈酸性,混合溶液中c(H+)=$\frac{0.032mol-0.03mol}{(0.06+0.04)L}$=0.2mol/L,pH=-lgc(H+)=-lg0.2=0.7,
答:混合溶液的pH=0.7;
(2)n[Ba(OH)2]=$\frac{2.1375g}{171g/mol}$=0.0125mol,n(BaSO4)=$\frac{1.165g}{233g/mol}$=0.005mol,根据S原子守恒得n(H2SO4)=n(BaSO4)=0.005mol,硫酸中n(H+)=2n(H2SO4)=2×0.005mol=0.01mol,
反应后溶液中pH=13,则溶液中c(OH-)=0.1mol/L,设盐酸中n(H+)为xmol,则$\frac{0.0125mol×2-0.01mol-xmol}{0.05L}$=0.1mol/L,x=0.01,
根据Cl、H原子守恒得n(Cl-)=n(HCl)=n(H+) (盐酸)=0.01mol,
c(SO42- )=$\frac{n}{V}$=$\frac{0.005mol}{0.05L}$=0.1mol/L,c(Cl-)=$\frac{0.01mol}{0.05L}$=0.2mol/L,
答:硫酸根离子、氯离子物质的量浓度分别是0.1mol/L、0.2mol/L.
点评 本题考查pH有关计算,为高频考点,侧重考查学生分析计算能力,正确判断物质之间的反应及溶液中存在的离子是解本题关键,注意(2)题盐酸、硫酸都和氢氧化钡反应,正确运用原子守恒,题目难度不大.


科目:高中化学 来源: 题型:解答题
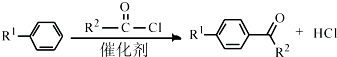 (R1、R2代表烷基)
(R1、R2代表烷基)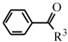 +ClCH2COOR4+R4ONa→
+ClCH2COOR4+R4ONa→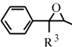 COOR4+R4OH+NaCl(R3、R4代表烷基)
COOR4+R4OH+NaCl(R3、R4代表烷基)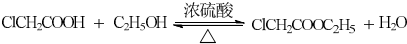 .
. .
.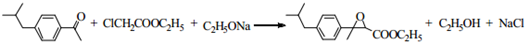 .
.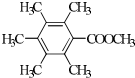 、
、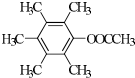 、
、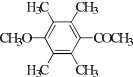 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
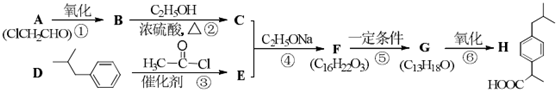
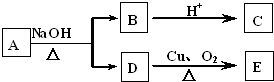 某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )
某有机物A的分子式为C6H12O2,已知A~E有如图转化关系,且D不与Na2CO3溶液反应,C、E均能发生银镜反应,则A的结构可能有( )| A. | 4种 | B. | 3种 | C. | 2种 | D. | 1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
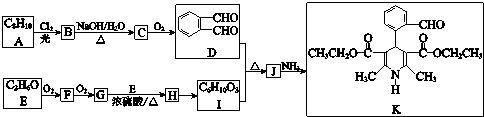
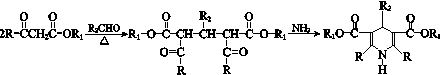
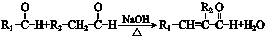 (R、R1、R2表示氢原子或烃基)
(R、R1、R2表示氢原子或烃基)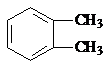 .
.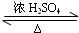 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.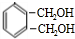 +O2 $→_{△}^{催化剂}$
+O2 $→_{△}^{催化剂}$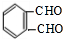 +2H2O.
+2H2O.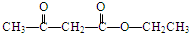 .
.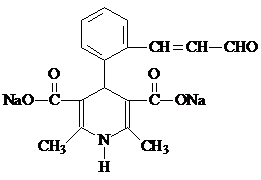 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | [NH4+]>[Cl-]>[OH-]>[H+] | B. | [NH4+]=[Cl-]>[H+]=[OH-] | C. | [Cl-]>[NH4+]>[OH-]>[H+] | D. | [OH-]>[NH4+]>[H+]>[Cl-] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常用的食品包装薄膜的主要成分是聚乙烯或聚氯乙烯塑料 | |
| B. | 食盐可作调味剂、食品防腐剂,还可用于调节体液电解质平衡 | |
| C. | 可利用米汤检验含碘盐的真假 | |
| D. | 利用厨房中的物品可以区别纯净的花生油与菜籽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL 2% H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5% H2O2溶液 | 1mL 0.1mol•L-1 FeCl3溶液 |
| 实验步骤 | 实验现象 | 实验结论 |
| 向盛有5mL 15%的H2O2溶液的试管中加入少量的HCl,然后把带火星的木条伸入试管中. | 无明显现象 | ①Cl-不具有催化作用或猜想3不正确 |
| 向盛有5mL 15%的H2O2溶液的试管中加入少量的FeCl3固体,然后把带火星的木条伸入试管中. | ②试管中有大量气泡产生,带火星的木条复燃 | ③Fe3+具有催化作用或猜想2正确 |
| 实验编号 | 温度/℃ | Na2S2O3 | V(H2SO4)/mL | V(H2O)/mL | |
| c/mol•L-1 | V/mL | ||||
| ① | 25 | 0.1 | 5.0 | 10.0 | a |
| ② | 25 | 0.1 | 10.0 | 10.0 | 0 |
| ③ | 25 | 0.1 | 5.0 | 5.0 | b |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
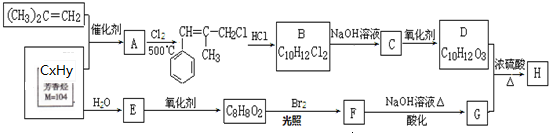
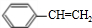
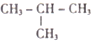 合成(CH3)2C=CH2的路线为:
合成(CH3)2C=CH2的路线为: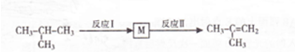 ,反应Ⅰ的条件为光照,写出反应Ⅱ的化学方程式
,反应Ⅰ的条件为光照,写出反应Ⅱ的化学方程式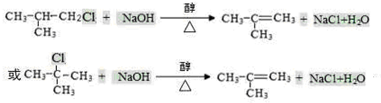
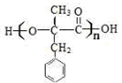
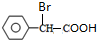 +2NaOH $→_{△}^{水}$
+2NaOH $→_{△}^{水}$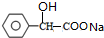 +NaBr+H2O
+NaBr+H2O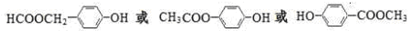 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )| A. | 在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=6时,c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1000 mol•Lˉ1 | |
| D. | pH=7时,消耗NaOH溶液的体积小于20.00mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com