


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、由C(石墨)=C(金刚石)△H=+1.90 kJ?mol-1 可知金刚石比石墨稳定 | B、在稀溶液中,H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热大于57.3 kJ | C、甲烷的标准燃烧热为△H=-890kJ?mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890 kJ?mol-1 | D、已知:H2(g)+F2(g)=2HF(g);△H=-270 kJ?mol-1,则1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
“西气东输”是西部开发的重点工程,这里的气是指天然气。工业上将碳与水在高温下反应制得水煤气,其中CO和H2的体积比为1∶1。
已知1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学反应方程式:
________________________________________________________________________________
1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量__________890 kJ(填“>”、“=”或“<”)。
(2)若忽略水煤气中的其他成分,在相同状况下要得到相等的热量,则所需水煤气与甲烷的体积比为__________;两者燃烧生成的CO2的质量之比为__________(前者比后者)。
(3)以上数据和计算说明,以天然气代替水煤气作民用燃料,突出的优点是_______________
_______________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(9分)“西气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,两者的体积比约为1∶1。已知1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学反应方程式:_____________________ ,
若1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量_______890 kJ(填“>”、“=”或“<”)。
(2)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为_______;燃烧生成的CO2的质量比约为_______。
(3)以上数据和计算说明,以天然气代替水煤气作民用燃料,突出的优点是___________。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山东省枣庄市高三3月模拟考试理综化学试卷(解析版) 题型:选择题
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g) +H2O(g)=CO(g) +3H2(g) △H>0,在一定条件下,向体积为1L的密闭容器中充入1 mol CH4 (g)和1mol H2O(g),测得H2O(g)和H2(g)的浓度随时间变化 曲线如图所示,下列说法正确的是
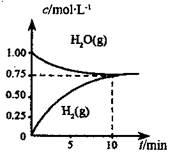
A.达平衡时,CH4( g)的转化率为75%
B.0~10 min 内,v(CO)=0.075 mol•L-1·min-1
C.该反应的化学平衡常数K=0.1875 mol•L-1
D.当CH4(g)的消耗速率与H2O(g)的生成速率相等,反应到达平衡
查看答案和解析>>
科目:高中化学 来源:2010-2011浙江省高一下学期期中考试化学试卷 题型:填空题
(9分)“西气东输”是西部开发的重点工程,这里的气是指天然气,其主要成分是甲烷。工业上将碳与水在高温下反应制得水煤气,水煤气的主要成分是CO和H2,两者的体积比约为1∶1。已知1 mol CO气体完全燃烧生成CO2气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量;1 mol CH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1)写出氢气完全燃烧生成液态水的热化学反应方程式:_____________________ ,
若1 mol CH4气体完全燃烧生成CO2气体和水蒸气,放出的热量_______890 kJ(填“>”、“=”或“<”)。
(2)忽略水煤气中其他成分,相同状况下若得到相等的热量,所需水煤气与甲烷的体积比约为_______;燃烧生成的CO2的质量比约为_______。
(3)以上数据和计算说明,以天然气代替水煤气作民用燃料,突出的优点是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com