
|


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为减缓反应速率,用饱和食盐水与电石反应制乙炔 |
| B、向苯中加入溴水可制取溴苯 |
| C、实验室制乙烯时应将无水乙醇缓慢加入浓硫酸中,并加入碎瓷片以防爆沸 |
| D、油脂在碱性条件下水解可以得到硬脂酸和甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 碱性 酸性 | AOH>BOH HC>HD | AOH<BOH HC>HD | AOH>BOH HC<HD | AOH<BOH HC<HD |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸镁 | B、氢氧化钠 |
| C、氨水 | D、碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
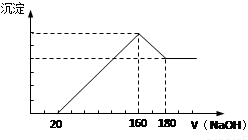
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热稳定性:NaHCO3>Na2CO3 |
| B、等物质的量浓度的Na2CO3溶液和NaHCO3溶液,前者pH小 |
| C、NaHCO3和Na2CO3的与等物质的量浓度的稀盐酸反应,NaHCO3反应速率更快 |
| D、等物质的量的NaHCO3和Na2CO3的与足量稀盐酸反应,NaHCO3放出的CO2多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com