
化合物ICl电子式 ,其中I的化合价为 ,你判断I化合价依据是 ,预测ICl与H2O反应的化学方程式为 。你预测反应正确与否的实验依据是
(提示:AgI为黄色沉淀)该反应 (填是/不是)氧化还原反应。次碘酸的电子式 。
(2)写出任意一种由多个原子组成的含有与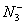 电子数相同的微粒的化学式 。
电子数相同的微粒的化学式 。
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.元素的种类由核外电子数决定
B.原子的种类由原子核内质子数与中子数共同决定
C.核外电子排布相同的两个粒子一定是同种原子
D.某元素的原子核内有m 个质子,n 个中子,则该元素的相对原子质量为m + n
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验室进行下列实验, 括号内的实验用品都能用到的是( )
A.硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体)
B.蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C.钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)
D.肥皂的制取(蒸发皿、玻璃棒、甘油)
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列事实得出的结论正确的是( )
A.试液 颜色无变化
颜色无变化 溶液变为血红色
溶液变为血红色
结论:试液中含有Fe2+
B.试液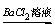 白色沉淀
白色沉淀 沉淀不溶解
沉淀不溶解
结论:试液中含有SO42-
C.某溶液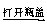 瓶口产生白雾
瓶口产生白雾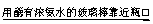 瓶口产生白烟
瓶口产生白烟
结论:此溶液一定为浓盐酸
D.无色试液 产生无色无味气体
产生无色无味气体 石灰水变浑浊
石灰水变浑浊
结论:原无色试液中一定含有CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
两种元素原子的核外电子层数之比与最外层电子数之比相等,则在核电荷数为1~18的元素中,满足上述关系的元素共有( )
A.3对 B.4对 C.6对 D.5对
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.1.0 mol·L-1KNO3溶液:H+,Fe2+,Cl-,SO4 2-
B.石蕊溶液呈红色的溶液:NH4+,Ba2+,AlO2-,Cl—
C.与铝反应产生大量氢气的溶液:Na+,K+,NH4+,NO3-
D.pH=12的溶液:K+,Na+,NO3—,Cl—
查看答案和解析>>
科目:高中化学 来源: 题型:
某电荷数小于18的元素X,其原子核外电子层数为a,最外层电子数为(2a+1)。下列有关元素X的说法中,不正确的是 ( )
A.元素X的原子核内质子数为(2a2-1)
B.元素X形成的单质既能作氧化剂又能作还原剂
C.元素X形成的简单离子,各电子层的电子数均达到2n2个(n表示电子层数)
D.由元素X形成的某些化合物,可能具有杀菌消毒的作用
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
(1)Al与NaOH溶液反应的离子方程式为 。
(2)下列实验能比较镁和铝的金属性强弱的是 (填序号)。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/LAlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al (s)+3O2(g) =2Al2O3(s) ΔH1 = -3352 kJ/mol
Mn(s)+ O2(g) =MnO2 (s) ΔH2 = -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是 。
(4)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,其反应方程式为 。
(5)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g)  Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0
某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是5.60g。
①H2的平均反应速率是 mol/(L·min)。
②若按n(SiCl4) : n(N2) : n(H2) = 3 : 2 : 6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应 (填“增大”、“减小”或“不变”)。
(6)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp= 。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10-5mol·L-1,需调节pH为______以上。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与反应Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
A.2Na2O2+2H2O =4NaOH+O2↑ B.Cl2 + H2O  HClO + HCl
HClO + HCl
C.2F2+2H2O=4HF+O2 D.4Fe(OH)2+O2+2H2O=4Fe(OH)3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com