
工业上有一种利用天然气合成氨的工艺,流程示意图如下:
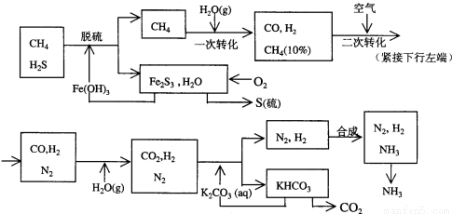
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是_____________________________;得到单质硫的化学方程式是________________________;
(2)为使K2CO3(aq)和CO2充分反应温度与压强应当如何控制,为什么?_________________;
(3)流程中有三处循环,分别是_________________;
(4)碳酸氢钾分解得到的CO2可用于_________________;
(5)一次转化后CO所占体积比是_________________;
(6)合成氨生产主要设备有_________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016届云南省高三下第七次月考理综化学试卷(解析版) 题型:填空题
高纯六水氯化锶晶体(SrCl2•6H2O)具有很高的经济价值,工业上用w kg难溶于水的的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),共制备高纯六水氯化锶晶体(a kg)的过程为:
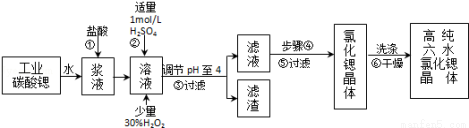
已知:Ⅰ.SrCl2•6H2O晶体在61℃时开始失去结晶水,100℃时失去全部结晶水.
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:

(1)操作①加快反应速率的措施有________________ (写一种)。操作①中盐酸能否改用硫酸,其理由是:
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为________.
(3)在步骤②﹣③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为________.
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是________ (填化学式).
(5)工业上完成操作③常用的设备有:
A分馏塔 B 离心机 C 热交换器 D 反应釜
(6)工业上用热风吹干六水氯化锶,适宜的温度是____________
A.40~50℃ B.50~60℃ C.60~70℃ D.80℃以上.
(7)已知工业流程中锶的利用率为90%根据以上数据计算工业碳酸锶的纯度:
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三考前热身(五模)化学试卷(解析版) 题型:选择题
下列有关物质的性质与其应用不相对应的是
A.Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品
B.二氧化硅有良好的导电性,是制造光导纤维的主要材料
C.药皂中加入少量苯酚,可以起到杀菌消毒的作用
D.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面的油污
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:选择题
下列离子方程式的书写中正确的是( )
A.将少量碳酸钠溶液滴加到盐酸中 CO32- +2H + =H2O+CO2↑
B.向明矾中加入氢氧化钡使硫酸根完全沉淀 Ba2+ +SO42- =BaSO4↓
C.苯酚钠中通入少量CO2 C6H5O - +CO2 +H2O→C6H5OH+HCO3 -
D.向石灰乳中通入过量的SO2 OH - +SO2=HSO3-
查看答案和解析>>
科目:高中化学 来源:2016届海南师大附中高三临考模拟化学试卷(解析版) 题型:选择题
正确使用化学用语是学好化学的基础。以下化学用语的使用中不正确的是( )
A.酒精的实验式为:C2H6O
B.原子核中有7个中子的碳原子:136C
C.铝离子的电子式:Al3+
D.二氧化硅的结构式O=Si=O
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三下冲刺模拟理综化学C卷(解析版) 题型:选择题
如图甲是一种利用微生物将废水中的尿素(H2NCONH2,氮元素显-3价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )
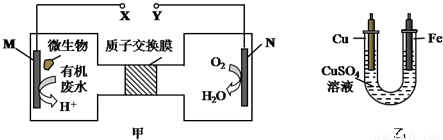
A.H+透过质子交换膜由左向右移动
B.铜电极应与Y相连接
C.M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+
D.当N电极消耗0.25mol气体时,则铁电极增重16g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高二6月月考化学试卷(解析版) 题型:填空题
1L某混合溶液,可能含有的离子如下表:
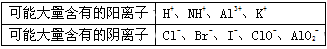
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。
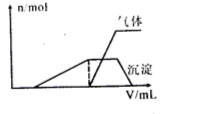
①则该溶液中一定含有的离子是 ;
②可能存在的阳离子有 ;
③肯定不存在的阴离子是 。
(2)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向2 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题。

①a的值为 ;
②当通入Cl2的体积为3.36 L(标准状态下)时,溶液中发生反应的离子方程式为 ;此时溶液中Br-、I-的物质的量浓度分别为c(Br-)= ,c(I-)= 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁沈阳二中高一6月月考化学试卷(解析版) 题型:填空题
Ⅰ甲醚作为一种基本化工原料,由于其良好的易压缩、冷凝、汽化特性,使甲醚在制药、燃料、农药等化学工业中有许多独特的用途。
(1)已知:2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ·mol-1,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:

①平衡时,c(CH3OCH3)等于________ mol·L-1,反应混合物的总能量减少________ kJ。
②若在平衡后的容器中再加入与起始时等量的CH3OH,请在下图中画出CH3OH的浓度的曲线示意图。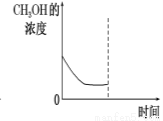
Ⅱ甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+ CO(g)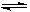 CH3OH(g)
CH3OH(g)
(2)下表所列数据是该反应在不同温度下的化学平衡常数(K)

①该反应的平衡常数表达式K= ,△H 0(填“>”、“<”或“=”).
②按下列物质的量发生反应,CO的转化率由大到小的顺序是 (填甲乙丙).

(3)已知在常温常压下:化学反应①②③④的平衡常数分别为K1,K2,K3,K4
①2CH3OH(l)+3O2(g)= 2CO2(g)+4H2O(g) K1
2CO2(g)+4H2O(g) K1
②2CO(g)+O2(g)=2CO2(g)K2
③H2O(g)=H2O(l)K3
④CH3OH(l)+O2(g)=CO(g)+2H2O(l)K4
则K4= (用含有K1,K2,K3的代数式表达)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁沈阳二中高二6月小班成果验收化学卷(解析版) 题型:选择题
下列说法不正确的是 ( )
A.云、烟、雾等均能产生丁达尔现象
B.PM2.5分散在大气中一般构不成胶体
C.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
D.用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com