
| A. | 它们都含有碳、而且碳原子有四个价电子,碳原子间以及碳与其他原子间结构多样 | |
| B. | 它们反应很复杂 | |
| C. | 制取它们的方法很多 | |
| D. | 它们都是非电解质 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
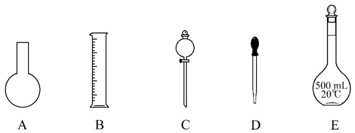
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.96% | B. | 5.66% | C. | 75% | D. | 12.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.7g | B. | 23.4 g | C. | 35.1g | D. | 58.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水无法鉴别乙醇、甲苯和溴苯 | |
| B. | 可用酸性高锰酸钾溶液除去甲烷中的乙烯 | |
| C. | C2H5OOCCOOC2H5的名称:二乙酸乙二酯 | |
| D. | 除去苯中的苯酚可加入氢氧化钠溶液后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
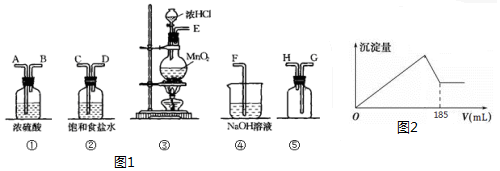
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石燃烧比石墨燃烧放出的热量少 | |
| B. | 等质量是石墨燃烧放热多 | |
| C. | 石墨的能量比金刚石的能量高 | |
| D. | 由石墨制备金刚石一定是吸热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com