


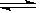 HPO4 2- + OH- (1分)
HPO4 2- + OH- (1分)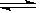 HPO4 2- + OH-
HPO4 2- + OH- 

科目:高中化学 来源:不详 题型:单选题
A.△H=△H1+
| B.△H=△H1+
| ||||||||
| C.△H=△H1+2△H2+2△H3 | D.△H=2△H1+△H2+△H3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.水是弱电解质 | B.可燃冰是可以燃烧的水 |
| C.氢氧两种元素只能组成水 | D.0℃时冰的密度比液态水的密度大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.含有NH4+、Cl-、H+、OH-离子的溶液中,其离子浓度一定是: c(Cl-)>c(NH4+)> c(H+)> c(OH-) |
| B.pH=6的醋酸与醋酸钠的混合溶液中c(Na+)>c(CH3COO-) |
| C.0.lmol/L的Na2S溶液中,c(OH-)= c(H+)+ c(HS-)+2 c(H2S) |
| D.pH=3的一种酸和pH=11的一种碱等体积混和后的溶液中一定是c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
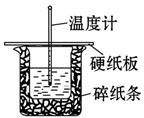
| A.小烧杯内残留有水,会使测得的反应热数值偏小 |
| B.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅 |
| C.烧杯间填满碎纸条的作用是固定小烧杯 |
| D.可用相同浓度和体积的硝酸代替稀盐酸溶液进行实验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是| A.将纯水加热到950C时,Kw变大,pH不变,水仍呈中性 |
| B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 |
| C.向纯水中加人少量固体碳酸钠,c(H+)减小,Kw不变,促进水的电离 |
| D.向纯水中加入醋酸钠或盐酸,均可抑制水的电离,Kw不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.滤液b的pH=7 |
| B.②中颜色变化说明Mg(OH)2转化为Fe(OH)3 |
| C.实验可以证明Fe(OH)3的溶解度比Mg(OH)2的小 |
D.浊液a中存在沉淀溶解平衡:Mg(OH)2(s) Mg2+(aq)+ 2OH-(aq) Mg2+(aq)+ 2OH-(aq) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 原料 | 天然气 | 重油 | 煤 |
| 相对投资费用 | 1.0 | 1.5 | 2.0 |
| 能量消耗/J·t-1 | 28×109 | 38×109 | 48×109 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com