
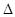 H<O��ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ����
H<O��ʵ���÷�Ӧ�����е�t minʱN2�����������ͼ��ʾ������˵����ȷ����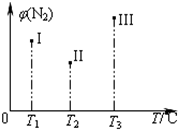
| A����z��v(H2)=3v(N2)ʱ������˵�����������еķ�Ӧ��ƽ��״̬ |
| B����t minʱ��һ���ﻯѧƽ��״̬���Ǣ�͢� |
| C����t minʱ��һ��û�дﻯѧƽ��״̬����I |
| D�����������еķ�Ӧ���ﵽƽ�������I�л�������ƽ����Է���������С |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����Ƶ���ˮ�ڹ�������ɫ��dz |
| B��H2��I2��HIƽ��������ѹ����ɫ���� |
| C���ϳ� NH3��Ӧ��Ϊ��� NH3�IJ��ʣ�������Ӧ��ȡ��Խϵ��¶ȵĴ�ʩ |
| D��ʵ�������ű���ʳ��ˮ��������ˮ���ռ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 3C(g)+D(g)���ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪWmol/L����
3C(g)+D(g)���ﵽƽ��ʱ��C��Ũ��ΪW mol/L����ά������������¶Ȳ��䣬���������ַ����ı���ʼ���ʣ��ﵽƽ���C��Ũ����ΪWmol/L����| A��4molA+2molB | B��2molA+1molB+3molC+1molD |
| C��3molC+1molD+1molB | D��3molC+1molD |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����ˮ����ƽ�⣺Cl2+H2O HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz |
B����CO(g)+NO2(g) CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� |
C����2NO2(g)  N2O4(g), �����¶�ƽ����ϵ��ɫ���� N2O4(g), �����¶�ƽ����ϵ��ɫ���� |
| D��SO2��������SO3�ķ�Ӧ��������������Ŀ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
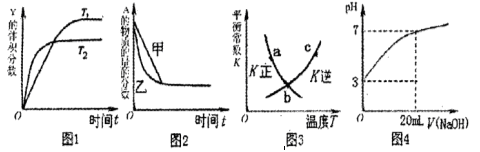
A��ͼ1��ʾ���淴Ӧ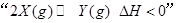 �¶� �¶�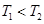 ������ ������ |
B��ͼ2��ʾѹǿ�Կ��淴Ӧ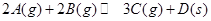 ��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� ��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ�� |
| C��ͼ3��a��b��c������ֻ��b���Ѿ��ﵽ��ѧƽ��״̬ |
| D��ͼ4����20mL pH=3�Ĵ�����Һ�еμ�pH=11��NaOH��Һ������pH�仯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 HBr+HBrO����Ҫʹ��ˮ����ɫ��dz���ɲ�ȡ�Ĵ�ʩ��
HBr+HBrO����Ҫʹ��ˮ����ɫ��dz���ɲ�ȡ�Ĵ�ʩ��| A����ѹ | B������NaF���� | C��ͨ��SO2���� | D������NaI���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 PCl5��g����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� ��
PCl5��g����ƽ��ʱ��PCl5Ϊ0.40 mol�������ʱ����1.0 mol PCl3��0.50 mol Cl2������ͬ�¶����ٴ�ƽ��ʱPCl5�����ʵ����ǣ� �� | A��0.40 mol | B��0.20 mol |
| C����0.20 mol | D������0.20 mol����0.40 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 �����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����
�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����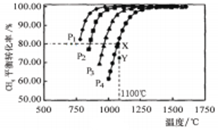
| A��������Ӧ�ġ�H>0 |
| B��ѹǿP1>P2>P3>P4 |
| C��1100��÷�Ӧ��ƽ�ⳣ��Ϊ64mol2��L-1 |
| D��ѹǿΪP4ʱ����Y�㣺v(��)<v(��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 I3-�ﵽƽ��ʱc(I3-)���¶ȵĹ�ϵ��ͼ��ʾ��
I3-�ﵽƽ��ʱc(I3-)���¶ȵĹ�ϵ��ͼ��ʾ��
| A��ͼ�з�Ӧ���е�״̬Dʱ��һ����v��>v�� |
| B��A���B��Ļ�ѧƽ�ⳣ����ͬ |
| C����B����Һ�����¶�ʱ���÷�Ӧ��v��>��v�� |
| D������KI��ҺŨ��������I2���ܽ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com