
分析 (1)依据蛋白质水解生成氨基酸解答;
(2)病人的尿液中葡萄糖含量是检测糖尿病指标;
(3)油脂在碱性环境下水解生成肥皂主要成分,高级脂肪酸盐;
(4)醋酸能够与碳酸钠反应生成醋酸钠和水、二氧化碳;
(5)乙醇可用于杀菌消毒;
(6)天然气主要成分为甲烷;
解答 解:(1)蛋白质水解生成氨基酸,故选:F;
(2)糖尿病通常是指病人的尿液中葡萄糖含量超标,故选:E;
(3)工业上制造肥皂的主要原料是油脂,油脂在碱性环境下水解生成肥皂主要成分,故选:D;
(4)醋酸能够与碳酸钠反应生成醋酸钠和水、二氧化碳,故选:C:
(5)乙醇可使蛋白质变性,常用于杀菌消毒,故选:B;
(6)天然气主要成分为甲烷,故选:A;
点评 本题考查较为综合,涉及有机物的组成、结构、性质和应用的考查,题目较为基础,注意相关知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | 稳定性:HCl>H2S>H2O | B. | 碱性:NaOH>KOH>Mg(OH)2 | ||
| C. | 酸性:HClO4>HBrO4>HIO4 | D. | 还原性:I-<Br-<Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的或结论 | |
| A | 蘸有浓硝酸的玻璃棒靠近浓氨水时冒白烟 | NH3具有还原性 |
| B | 将一块Na放入乙醇溶液中,有气泡产生 | Na能置换乙醇中的氢 |
| C | 可将58.5gNaCl加入盛有500mL水的烧杯中,搅拌、溶解 | 粗略配置浓度为2mol•L-1的NaCl溶液 |
| D | 向氯仿中加入NaOH溶液,加热充分反应后,再加入AgNO3 | 验证氯仿中含有的氯元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4-、Al3+ | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32-、CO32- | |
| C. | 含有大量AlO2-的溶液中:K+、HCO3-、Br-、Na+可共存 | |
| D. | 在某钠盐溶液中含有等物质的量的Cl-、I-、AlO2-、CO32-、NO3-、SiO32-中若干种,当加入过量的盐酸产生气泡,溶液颜色变深,最终溶液中无沉淀,阴离子种数减少3种,则原溶液中一定有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3g钠由原子变成离子时,失去的电子数为0.2 NA | |
| B. | 0.2 NA个硫酸分子与19.6g磷酸(H3PO4)含有相同的氧原子数 | |
| C. | 28g氮气所含的原子数为NA | |
| D. | NA个氧分子与NA个氢分子的质量比为8:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (Υ1+Υ2-Υ3)L | B. | (Υ1+Υ2+Υ3)L | C. | (Υ1+Υ2-2Υ3)L | D. | [Υ3-(Υ1+Υ2)]L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
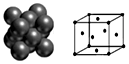 铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题:
铁、铝、铜都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.请回答以下问题: ;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).
;NH4CuSO3中N、S、O三种元素的第一电离能由大到小的顺序为N>O>S(元素符号表示).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com