
| A、向小苏打溶液中加入醋酸溶液:HCO3-+H+=CO2↑+H2O |
| B、氢氧化镁与稀硫酸反应:H++OH-=H2O |
| C、钠与水反应,有氢气产生:Na+H2O=Na++OH-+H2↑ |
| D、碳酸钙与盐酸反应:CaCO3+2H+=Ca2++H2O+CO2↑ |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| 实验目的 | 试剂及方法 |
| 鉴别CuSO4、Na2SO4两种粉末 | |
| 检验自来水中是否含有Cl- | |
| 证明Na2CO3溶液具有碱性 | |
| 除去镁粉中混有少量的铝粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
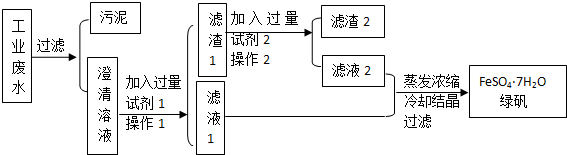
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述反应中,1mol N2被氧化时,可以得到6mol电子 |
| B、上述反应中,被氧化与被还原的物质 物质的量之比为2:3 |
| C、每生成1mol AlN时.消耗N2的质量为14g |
| D、AlN的摩尔质量为41g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯中碳碳双键的键能是乙烷中碳碳单键的键能的2倍 |
| B、N-O键的极性比C-O键的极性大 |
| C、氮气分子中含有1个σ键和2个π键 |
| D、NH4+中4个N-H键的键能不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只存在于氧气中 |
| B、只存在于SO3中 |
| C、只存在于SO2和SO3中 |
| D、SO2、SO3、O2中都存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、锂电极发生氧化反应 |
| B、电子从锂电极通过外电路流向碳电极 |
| C、每生成1mol SO2转移4mol电子 |
| D、SOCl2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(H+)=1×10-13mol?L-1的溶液:Na+、Ba2+、HCO3-、SO42- |
| B、加入铝单质能产生大量氢气的溶液:Na+、NO3-、SO42-、Cl- |
| C、在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
| D、在能使紫色的石蕊试液变红的溶液中:Na+、NH4+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温 | B、增大反应器体积 |
| C、增大c(A) | D、降温 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com