
 ,CO的结构可以表示为
,CO的结构可以表示为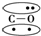 ,其中椭圆框表示π键,下列说法中不正确的是( )
,其中椭圆框表示π键,下列说法中不正确的是( )| A. | N2分子与CO分子中都含有叁键 | B. | CO分子中有一个π键是配位键 | ||
| C. | N2与CO互为等电子体 | D. | N2与CO的化学性质相同 |
分析 A.根据图象知,氮气和CO都含有两个π键和一个σ键;
B.CO分子中其中一个π键由O原子提供1对电子形成;
C.原子总数相同、价电子总数也相同的微粒互为等电子体;
D.N2分子与CO分子的化学性质不相同.
解答 解:A.根据图象知,氮气和CO都含有两个π键和一个σ键,N2分子与CO分子中都含有三键,故A正确;
B.氮气中π键由每个N原子各提供一个电子形成,而CO分子中其中一个π键由O原子提供1对电子形成属于配位键,故B正确;
C.N2分子与CO分子中原子总数相同、价电子总数也相同,二者互为等电子体,故C正确;
D.N2分子与CO分子的化学性质不相同,故D错误,
故选D.
点评 本题考查化学键、等电子体等,题目难度不大,侧重考查学生对化学键的理解.


科目:高中化学 来源: 题型:选择题
| A. | 0.1molNa与足量O2反应,转移0.2nA个电子 | |
| B. | 1L0.1mol•L-1Na2S溶液中含有0.1nA个S2- | |
| C. | 常温下,44gCO2含有nA个C原子 | |
| D. | 标准状况下,22.4L的CCl4含有4nA个Cl原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①③④⑥ | C. | ①②④⑥ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 Al(OH)3+OH-.
Al(OH)3+OH-.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 合金是重要的金属材料.
合金是重要的金属材料.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com