
【题目】如图所示,A、B、C三个装置中的烧杯分别盛有足量的CuCl2溶液。
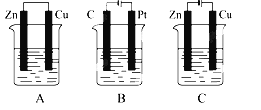
(1)A、B、C三个装置中属于原电池的是________(填标号)。
(2)A池中Zn极发生______反应(填“氧化”或“还原”);Cu是________极,该极的电极反应式为______________________。
(3)B池中Pt是____极,该极的电极反应为________, B池中总反应的化学方程式为________________________________,溶液中阴离子向________(C、Pt)极移动。
(4)C池中Cu极的电极反应为________________,反应过程中,溶液浓度________(填“变大”“变小”或“不变”)。
【答案】A 氧化 正 Cu2++2e-=Cu 阳 2Cl--2e-= Cl2↑ CuCl2![]() Cu+Cl2↑ Pt Cu_2e-= Cu2+ 不变
Cu+Cl2↑ Pt Cu_2e-= Cu2+ 不变
【解析】
(1)把化学能转化为电能的装置是原电池;把电能转化为化学能的装置是电解池,所以电解池有外接电源;
(2)该装置是原电池,较活泼的金属锌作负极,较不活泼的金属铜作正极,锌和氯化铜发生置换反应;
(3)电解池阴极上得电子发生还原反应,惰性材料作电极时,溶液中阴阳离子放电,阳极上氯离子放电,阴极上铜离子放电生成铜;
(4)连接原电池正极的是阳极,连接原电池负极的是阴极,阳极是活泼电极,电解池工作时,阳极材料失电子而不是溶液中阴离子失电子,根据阴阳极上发生的反应确定溶液中铜离子浓度是否变化。
(1)A装置是将化学能转化为电能的装置,为原电池;BC装置都有外接电源,所以是把电能转化为化学能的装置,属于电解池,故选A;
(2)该装置是原电池,较活泼的金属锌作负极,铜作正极,锌和铜离子发生氧化还原反应生成锌离子和铜单质,所以A池中Zn极发生失电子的氧化反应;Cu是正极,正极上铜离了得电子产生铜单质,反应的电极反应式为Cu2++2e-=Cu;
(3)B池中Pt连接电源的正极,是电解池的阳极,阳极上氯离子失电子产生氯气,电极反应为2Cl--2e-= Cl2↑, 阴极上铜离子得电子产生铜单质,B池中总反应的化学方程式为CuCl2![]() Cu+Cl2↑,溶液中阴离子向阳极,即Pt极移动;
Cu+Cl2↑,溶液中阴离子向阳极,即Pt极移动;
(4)C池中Cu极电源的正极,为阳极,阳极上铜失电子产生铜离子,电极反应为Cu_2e-= Cu2+,阴极上溶液中的铜离子得电子产生铜单质,为在锌上镀铜,反应过程中,溶液浓度不变。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】钼酸钠晶体(Na2MoO4·2H2O)是一种金属腐蚀抑制剂。工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图所示。
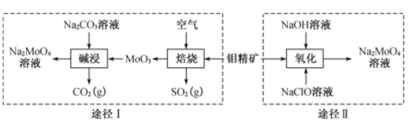
(1)NaClO的电子式为 ___。
(2)途径Ⅰ碱浸时发生反应的化学方程式为____。
(3)途径Ⅱ氧化时还有Na2SO4生成,则反应的离子方程式为____。
(4)已知途径Ⅰ的钼酸钠溶液中c(MoO42-)=0.40mol/L,c(CO32-)=0.10mol/L。由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-。当BaMoO4开始沉淀时,CO32-的去除率是______[已知Ksp(BaCO3)=1×10-9、Ksp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]。
(5)分析纯钼酸钠常用钼酸铵[(NH4)2MoO4]和氢氧化钠反应来制取,若将该反应产生的气体与途径Ⅰ所产生的气体一起通入水中,得到正盐的化学式是_______。
(6)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图
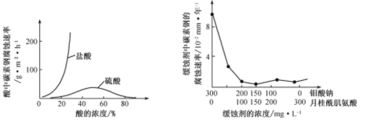
①当硫酸的浓度大于90%时,碳素钢腐蚀速率几乎为零,原因是____。
②若缓蚀剂钼酸钠-月桂酸肌氨酸总浓度为300mg·L-1,则缓蚀效果最好时钼酸钠(M =206g·mol-1) 的物质的量浓度为____(计算结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,1-二环丙基乙烯(![]() )是重要医药中间体,下列关于该化合物的说法正确的是
)是重要医药中间体,下列关于该化合物的说法正确的是
A.所有碳原子可能在同一平面B.乙苯与它互为同分异构体
C.二氯代物有9种D.只能发生取代、加成、加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是( )
A.砷原子的结构示意图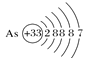 B.BF4—的结构式
B.BF4—的结构式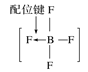
C.HF分子间的氢键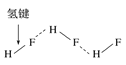 D.丙氨酸的手性异构
D.丙氨酸的手性异构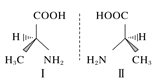
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学按如图所示实验装置探究铜与浓硫酸的反应,记录实验现象如表。下列说法正确的是
试管 | ① | ② | ③ | ④ |
实验现象 | 溶液仍为无色,有白雾、白色固体产生 | 有大量白色沉淀产生 | 有少量白色沉淀产生 | 品红溶液褪色 |

A.②中白色沉淀是BaSO3
B.①中可能有部分浓硫酸挥发了
C.为了确定①中白色固体是否为硫酸铜,可向冷却后的试管中注入水,振荡
D.实验时若先往装置内通入足量N2,再加热试管①,实验现象不变
查看答案和解析>>
科目:高中化学 来源: 题型:
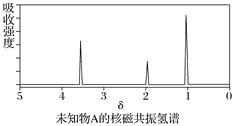
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的有( )
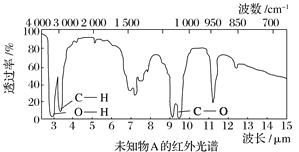
A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子
C. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
D. 仅由其核磁共振氢谱无法得知其分子中的氢原子总数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿酸是合成青蒿素的原料,可以由香草醛合成:

下列有关叙述正确的是
A. 香草醛的分子式是C8H10O3
B. 香草醛能与NaHCO3溶液反应
C. 两种物质均可与溴的四氯化碳溶液发生加成反应
D. 可用FeCl3溶液检验青蒿酸中是否含香草醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:在淀粉-碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:向实验①的溶液中加入4mL 0.5 mol·L-1的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式:____。
(2)实验②的化学反应中转移电子的物质的量是____。
Ⅱ.(3)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂。等物质的量的上述物质消毒效率最高的是____(填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是____(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几组物质,请将序号填入下列空格内:
A.苯和乙苯 B.12C60和石墨 C.![]() 和
和![]() D.35Cl和37Cl E.乙酸和乙二酸
D.35Cl和37Cl E.乙酸和乙二酸
(1)互为同位素的是___;
(2)互为同系物的是___;
(3)互为同素异形体的是__;
(4)互为同分异构体的是___;
(5)既不是同系物,又不是同分异体,也不是同素异形体,但可看成是同一类物质的是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com