
【题目】下列有关物质分类的叙述正确的是( )
A.CaCl2、NaOH、HCl、O2四种物质都属于化合物
B.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
C.溶液、浊液、胶体都属于混合物
D.CO2、CO等非金属氧化物均属于酸性氧化物
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将2.5gNaHCO3、Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是
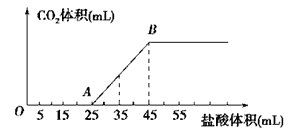
A. OA段发生反应的离子方程式为:OH-+H+==H2O H++CO32-==HCO3-
B. 当加入35mL盐酸时,产生CO2的体积为336mL
C. 混合物中NaOH的质量0.6g
D. A点溶液中的溶质为NaCl、NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 测定等物质的量浓度的Na2CO3和Na2SO4溶液的pH,前者的PH比后者的大 | 元素非金属性:S>C |
B | 向盛有Fe(NO3)2溶液的试管中加入0.lmol.L-1H2SO4溶液,试管口出现红棕色气体 | 溶液中NO3-被Fe2+还原为NO2 |
C | 向FeBr2溶液中加入少量氯水,再加CCl4萃取,CCl4层无色 | Fe2+的还原性强于Br- |
D | 向溶液中滴加盐酸酸化的BaC12溶液,产生白色沉淀 | 溶液中一定含有SO42- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菠菜具有丰富的营养。民间流传:菠菜与豆腐不宜同时食用。
资料:(1)菠菜中含有可溶性草酸盐、碳酸盐等
(2)醋酸不与草酸钙反应
(3)某草酸钙晶体(CaC2O4·xH2O)的相对分子质量为128+18x
【实验一】菠菜中部分成分分析

(1)用开水煮沸菠菜样品碎末2~3 min的目的是___________________。
(2)溶液M中含有的主要阴离子有____________________。
(3)已知C能使澄清石灰水变浑浊。A与醋酸生成C的化学方程式是__________。
(4)B的化学式可能是________________。
(5)草酸比碳酸的酸性___________(填“强”或“弱”)。
【实验二】对某草酸钙晶体进行热分解研究,得到相关数据如图所示。

(1)800℃时得到的固体只含钙元素和氧元素,质量比为5:2,其化学式是__________。
(2)固体质量由12.8 g变为10.0 g的过程中发生反应的化学方程式是__________。
(3)x =_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸锰(MnCO3) 是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。
(1) 工业上制备方程式为:MnSO4+2NH4HCO3=MnCO3 ↓+ (NH4)2SO4+CO2 ↑+H2O。反应中通常需加入稍过量的NH4HCO3,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是_____。
(2) 实验室模拟工业二氧化锰制备硫酸锰装置如图4所示。

①石灰乳的作用是________。
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有________。
(3) MnCO3 在空气中加热易转化为不同价态的锰的氧化物,且其固体残留率随温度的变化如图5 中A、B、C、D 点所示。则300℃时,剩余固体中锰元素与氧元素的物质的量之比即n(Mn) :n(O)为_______; 图中点D 对应固体的成分为______ (填化学式)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下,回答下列问题:
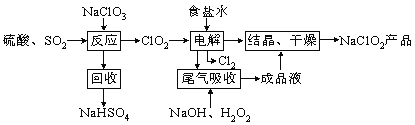
(1)ClO2的沸点为283K,纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下更安全。写出“反应”步骤中生成ClO2的化学方程式 。
(2)“尾气吸收”是吸收“电解”过程排出的少量ClO2。
①在尾气吸收过程中,可代替H2O2的试剂是 (填序号)。
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
②提高尾气的吸收效率的可行措施有 (填序号)。
A.尾气吸收时充分搅拌吸收液 B.适当加快尾气的通入速率
C.将温度控制在20℃以下 D.加水稀释尾气吸收液
③此吸收反应中,氧化剂与还原剂的物质的量之比为 。
(3)在碱性溶液中NaClO2比较稳定,在酸性溶液中,ClO2-和H+结合为HClO2,HClO2是唯一的亚卤酸,不稳定,易分解产生Cl2、ClO2和H2O,写出HClO2分解的化学方程式: 。
(4)已知NaClO2的溶解度随温度升高而增大,NaClO2饱和溶液在38℃以上60℃以下会析出NaClO2,在NaClO2析出过程中可能混有的杂质是 (填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化不能通过一步化学反应实现的是( )
A.BaCl2→BaSO4B.CuO→Cu(OH)2
C.NaOH→Na2CO3D.MgSO4→Mg(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的化合物A存在如下转化关系:

已知B为黄绿色气体单质。请完成下列问题:
(1)A的化学式________。
(2)向C的溶液中滴加适量KSCN溶液,无明显现象,再滴加几滴B的水溶液,溶液呈血红色。 用离子方程式表示该过程________、________。
(3)若D为金属,则D的化学式________ (写出2种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com