
| A�� | ��Ũ��Ϊ0.1 mol/L ��FeI2��Һ��ͨ��Cl2��Fe2+�ȷ�Ӧ | |
| B�� | ��NH4Al��SO4��2��Һ�еμ�������NaOH��Һ��NH4+�ȷ�Ӧ | |
| C�� | ��Ũ�Ⱦ�Ϊ0.1 mol/L��Na2CO3��NaOH�����Һͨ��CO2���壬NaOH�ȷ�Ӧ | |
| D�� | ���Ũ�ȵ�FeCl3��Һ������������ҿ�����С��ͬ������ͭ��ͭ�ȷ�Ӧ |
���� A�����ݵ����ӵĻ�ԭ�Դ��ڶ������жϣ�
B���������������백ˮ��Ӧ�����������������жϣ�
C������̼���������������Ʒ�Ӧ����̼�����жϣ�
D������ͭ���ã�
��� �⣺A����Ϊ�����ӵĻ�ԭ�Դ��ڶ�������������Ũ��Ϊ0.1 mol/L ��FeI2��Һ��ͨ��Cl2��I-�ȷ�Ӧ����A����
B����Ϊ���������백ˮ��Ӧ������������������������NH4Al��SO4��2��Һ�еμ�������NaOH��Һ���������ȷ�Ӧ��������������������B����
C����Ϊ̼���������������Ʒ�Ӧ����̼���ƣ�����Na2CO3��NaOH�����Һͨ��CO2���壬NaOH���������̼��Ӧ����̼������Һ����C��ȷ��
D������ͭ���ã��������Ũ�ȵ�FeCl3��Һ������������ҿ�����С��ͬ������ͭ�����ȷ�Ӧ����D����
��ѡC��
���� ���⿼�����ʵ����ʣ���Ŀ�ѶȲ���ע��������ʵ�����Ϊ��������Ŀ�Ĺؼ���


 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼������Һ���ݹ�¯ˮ����CaSO4+CO32-�TCaCO3��+SO42- | |
| B�� | �Ȼ�ѧ����ʽC2H2��g��+$\frac{5}{2}$O2��g���T2CO2��g��+H2O��g������H=-1256kJ/mol����ʾ��Ȳ��ȼ����Ϊ1256kJ/mol | |
| C�� | ���缫���MgCl2������Һ��MgCl2$\frac{\underline{\;���\;}}{\;}$Mg+Cl2�� | |
| D�� | H+��aq��+OH��aq���TH2O��1������H=-57.3 kJ/mol����ʾ��1 mol NaOH������������Һ�뺬0.5 mol H2SO4��Ũ�����Ϻ�ų�57.3 kJ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƽ� | B�� | ��ͭ | C�� | ���� | D�� | ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2O3 | B�� | Fe��OH��3 | C�� | FeO | D�� | Fe3O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
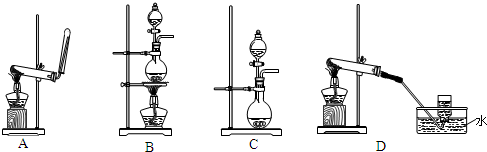
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�䣨h�� | ��ʼ | 8 | 16 | 24 | 32 | 40 | 48 |
| pH | 5.0 | 4.8 | 4.5 | 4.3 | 4.2 | 4.0 | 4.0 |
| ��� | ʵ�� | ���� |
| a | ��������ˮ | ľ��ȼ�� |
| b | ����Na2SiO3������Һ | ľ����ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
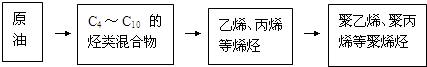
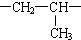 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | T/K | п��� | ����Ũ��/mol•L-1 | ʵ��Ŀ�� |
| �� | 298 | �ֿ��� | 2.00 | ����ʵ��ٺ͢�̽������Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻����ʵ��ٺ� ��̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻����ʵ��ٺ� ��̽��п��֡�ϸ���Ը÷�Ӧ���ʵ�Ӱ�죮 |
| �� | 298 | |||
| �� | 308 | |||
| �� | 298 |
| ʱ�䣨S�� | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| ���������mL�� | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 17g �������е�ԭ������ΪNA | |
| B�� | 2.4 g ����þ��������ȫ��Ӧʱʧȥ��������ΪNA | |
| C�� | ���³�ѹ�£�6.4 g ��������������������ԭ����Ϊ0.2 NA | |
| D�� | ���³�ѹ�£�11.2 L �������еķ�����Ϊ0.5 NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com