
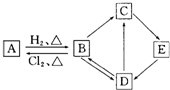
 图中的每一方格表示相关的一种反应物或生成物.其中B是一种单质,其余物质也都是有B元素的化合物.C是一种钠盐,E是C的对应的酸,B的结构类似金刚石,D为B的氧化物(其他不含B元素的反应产物以及各步反应添加的必要试剂和反应条件已被略去),请填写空白:
图中的每一方格表示相关的一种反应物或生成物.其中B是一种单质,其余物质也都是有B元素的化合物.C是一种钠盐,E是C的对应的酸,B的结构类似金刚石,D为B的氧化物(其他不含B元素的反应产物以及各步反应添加的必要试剂和反应条件已被略去),请填写空白:分析 B是一种单质,其余物质都是含有B元素的化合物,B的结构类似金刚石,A与B之间转化为硅的提纯,则B为Si,A为SiCl4,D为B的氧化物,则D是SiO2,C是一种钠盐,则C是Na2SiO3,E是C对应的酸,则E是H2SiO3,再结合物质性质解答.
解答 解:B是一种单质,其余物质都是含有B元素的化合物,B的结构类似金刚石,A与B之间转化为硅的提纯,则B为Si,A为SiCl4,D为B的氧化物,则D是SiO2,C是一种钠盐,则C是Na2SiO3,E是C对应的酸,则E是H2SiO3.
(1)A、D、E的化学式分别为:SiCl4、SiO2、H2SiO3,
故答案为:SiCl4;SiO2;H2SiO3;
(2)A和B的互转在工业上实际意义:粗硅提纯,
故答案为:粗硅提纯;
(3)E→D反应的化学方程式:H2SiO3 $\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O,
故答案为:H2SiO3 $\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O.
点评 本题考查无机物推断,涉及硅元素单质及其化合物性质与转化,熟练掌握常见元素化合物知识,注意工业上粗硅提纯.


科目:高中化学 来源: 题型:选择题
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
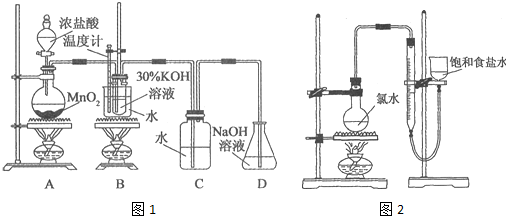
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.2mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
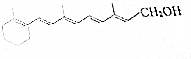 维生素A(见图)是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致夜盲症、皮肤干燥等多种病症.
维生素A(见图)是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致夜盲症、皮肤干燥等多种病症.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放电时,LiMn2O4发生氧化反应 | |
| B. | 放电时.正极反应为Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 充电时.LiMn2O4发生氧化反应 | |
| D. | 锂离子电池的比能量(单位质量释放的能量)低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com