
| A. | v(Fe)=0.5mol/(L•min) | B. | v(H2SO4)=0.5mol/(L•min) | ||
| C. | v(H2)=0.5mol/(L•min) | D. | v(FeSO4)=0.5mol/(L•min) |
分析 2min时铁粉刚好溶解,n(Fe)=$\frac{5.6g}{56g/mol}$=0.1mol,则消耗硫酸为0.1mol,生成硫酸亚铁、氢气均为0.1mol,结合v=$\frac{△c}{△t}$ 计算.
解答 解:2min时铁粉刚好溶解,n(Fe)=$\frac{5.6g}{56g/mol}$=0.1mol,
A.Fe为纯固体,不能表示反应速率,故A错误;
B.消耗硫酸为0.1mol,则v(H2SO4)=$\frac{\frac{0.1mol}{0.1L}}{2min}$=0.5 mol/(L.min),故B正确;
C.该反应为溶液中的反应,无法表示氢气的浓度变化,故C错误;
D.v(FeSO4)=v(H2SO4)=$\frac{\frac{0.1mol}{0.1L}}{2min}$=0.5 mol/(L.min),故D正确;
故选BD.
点评 本题考查化学反应速率的计算及化学计量数与反应速率的关系,侧重反应中物质的状态及速率的计算公式的考查,注重基础知识的考查,选项AC为易错点,题目难度不大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
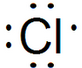 .
.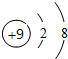 .
.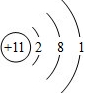 D2-的电子式为
D2-的电子式为 .
. ;Z元素原子的电子式为
;Z元素原子的电子式为 .
.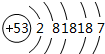 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | NaCl的电子式: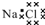 | ||
| C. | Cl-的结构示意图: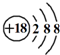 | D. | CH4的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
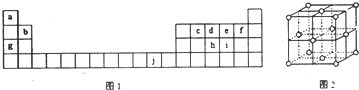
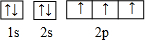 .
.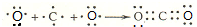 ,1molce2含有σ键的数目为6.02×1023.
,1molce2含有σ键的数目为6.02×1023.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| B. | 0.1mol/L NH4Cl溶液:c(NH4+)=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 在25℃时,将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后:c(H+)=c(CH3COO-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 剩余固体中一定含Fe | B. | 剩余固体中一定含Fe和Cu | ||
| C. | 剩余固体中一定不含Cu | D. | 剩余固体中一定含Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HBr、HCl、AgCl | B. | CaCO3、CH3COONa、NaHSO4 | ||
| C. | HClO、HF、NH3 | D. | H2CO3、CH3COOH、H2S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com