
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | ||
B、标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| C、pH=13的NaOH溶液中含有的OH-为0.1mol | ||
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4 |


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
| A、生铁比纯铁容易生锈 |
| B、钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 |
| C、钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-═4OH- |
| D、为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
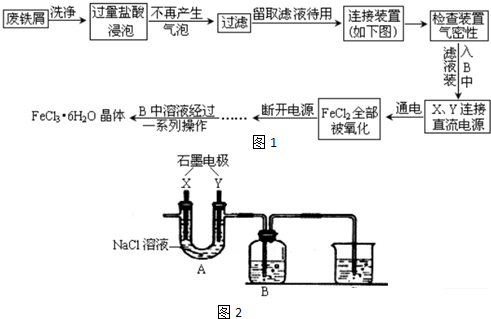
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Ba(OH)2溶液中滴加NaHSO4至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B、硫化钠溶液显碱性的原因:S2-+2H2O=H2S+2OH- |
| C、向碳酸钠溶液中通入少量的二氧化硫:2SO2+CO32-+H2O=2HSO3-+CO2↑ |
| D、氯化亚铁溶于稀硝酸中;3FeO+NO3-+10H+=3Fe3++NO↑+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、用锌粒与稀硫酸制取并收集H2 |
| B、用生石灰和浓氨水制取并收集NH3 |
| C、用少量MnO2和H2O2制取并收集O2 |
| D、用浓硫酸和浓盐酸制取并收集HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com