
【题目】(有机化学基础题)已知:![]() (主要产物),1 mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下所示的一系列变化。
(主要产物),1 mol某烃A充分燃烧后可以得到8 mol CO2和4 mol H2O。该烃A在不同条件下能发生如下所示的一系列变化。
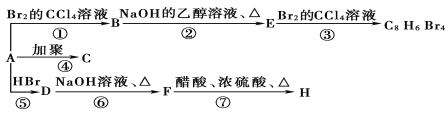
(1)A的化学式: ,A的结构简式: 。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出C、D、E物质的结构简式:
C ;D ;E
(4)写出D→F反应的化学方程式 。F (填“能”或“不能”)被Cu催化氧化。
【答案】(1)C8H8;![]() ; (2)加成;酯化
; (2)加成;酯化
(3)C为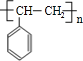 ,D为
,D为![]() ,E为
,E为![]()
(4)反应方程式为: 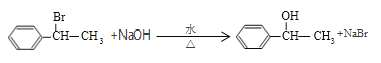 (3分);
(3分);
能
【解析】
试题分析: 1mol某烃A充分燃烧后可以得到8molCO2和4molH2O,故烃A的分子式为C8H8,不饱和度为(2×8+2-8)/2=5,可能含有苯环,由A发生加聚反应生成C,故A中含有不饱和键,故A为![]() ,C为
,C为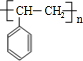 ,A与溴发生加成反应生成B,B为
,A与溴发生加成反应生成B,B为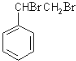 ,B在氢氧化钠醇溶液、加热条件下发生消去反应生成E,E为
,B在氢氧化钠醇溶液、加热条件下发生消去反应生成E,E为![]() ,E与溴发生加成反应生成
,E与溴发生加成反应生成![]() ,由信息烯烃与HBr的加成反应可知,不对称烯烃与HBr发生加成反应,H原子连接在含有H原子多的C原子上,
,由信息烯烃与HBr的加成反应可知,不对称烯烃与HBr发生加成反应,H原子连接在含有H原子多的C原子上,![]() 与HBr放出加成反应生成D,D为
与HBr放出加成反应生成D,D为![]() ,
,![]() 在氢氧化钠水溶液、加热条件下发生水解反应生成F,F为
在氢氧化钠水溶液、加热条件下发生水解反应生成F,F为![]() ,
,![]() 与乙酸发生酯化反应生成H,H为
与乙酸发生酯化反应生成H,H为![]() ,则
,则
(1)由上述分析可知,A的化学式为C8H8,结构简式为![]() 。(2)上述反应中,反应①是
。(2)上述反应中,反应①是![]() 与溴发生加成反应生成
与溴发生加成反应生成 ,
,
反应⑦是![]() 与乙酸发生酯化反应生成
与乙酸发生酯化反应生成![]() ,故答案为:加成;酯化;
,故答案为:加成;酯化;
(3)由上述分析可知,C为 ,D为
,D为![]() ,E为
,E为![]() ,H为
,H为![]() 。(4)D→F是
。(4)D→F是![]() 在氢氧化钠水溶液、加热条件下发生水解反应生成
在氢氧化钠水溶液、加热条件下发生水解反应生成![]() ,反应方程式为:
,反应方程式为:


科目:高中化学 来源: 题型:
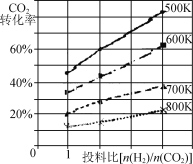
【题目】在体积可变的恒压密闭容器中反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。已知在压强p下,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图所示,则下列说法不正确的是( )
CH3OH(g)+H2O(g)。已知在压强p下,该反应在不同温度、不同投料比时,达平衡时CO2的转化率如图所示,则下列说法不正确的是( )
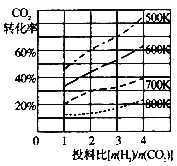
A.该反应的S<0,H<0
B.若温度不变,减小反应物投料比[n(H2)/n(CO2)],K值增大
C.700K投料比[n(H2)/n(CO2)] = 2时,达平衡时H2的转化率为45%
D.700K时,用平衡分压代替平衡浓度表示的化学平衡常数KP= ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e五种短周期元素的原子序数逐渐增大。a为非金属元素,且a、e同主族,c、d为同周期的相邻元素。e原子的质子数等于c、d原子最外层电子数之和。b原子最外层电子数是内层电子数的2倍。c的气态氢化物分子中有3个共价键。试推断:
(1)写出b元素在周期表中的位置 ;
(2)写出一种由a、c、d所形成的离子化合物 (化学式),它与e的最高价氧化物对应水化物的溶液加热时反应的离子方程式是 ;
(3)c的单质的电子式为 。
(4)b的最简单气态氢化物的结构式是
(5)b和d相比,非金属性较强的是 (用元素符号表示),下列事实能证明这一结论的是 (选填字母序号)。
A.常温下,b的单质呈固态,d的单质呈气态 |
B.d的氢化物的稳定性强于b的氢化物 |
C.b与d形成的化合物中,b呈正价 |
D.d的氢化物的沸点高于b的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌 (ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。

(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为________;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
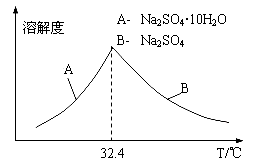
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备溴苯的实验装置如下图,将液溴从恒压滴液漏斗慢慢滴入盛有苯和铁粉的烧瓶A。反应结束后,对A中的液体进行后续处理即可获得溴苯。

(1)写出A中制备溴苯的化学反应方程式 。
(2)B中盛放的CCl4的作用是 。
(3)冷凝管的作用是 ,冷凝管中的水应从 口进入(填“a”或“b”)。
(4)向C中加入硝酸银溶液可证明苯和液溴发生的是取代反应而不是加成反应,反应现象是 ,也可使用 试纸更简便地证明上述结论。
(5)得到粗溴苯后,要用如下操作精制:①蒸馏 ②水洗 ③用干燥剂干燥 ④10%NaOH溶液洗,正确的操作顺序是 (填字母标号)。
a.①②③④② b.②④②③① c.④②③①② d.②④①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—-选修2:化学与技术】
甘氨酸亚铁络合物[化学式为(NH2CH2COO)2Fe]是常用的补铁剂,其合成方法如下:
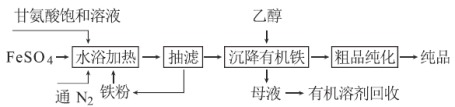
(1)通入N2的作用是 。
(2)已知甘氨酸显弱酸性,其结构简式为NH2CH2COOH,甘氨酸亚铁络合物易溶于水且在水中难电离,写出“水浴加热”过程中生成甘氨酸亚铁络合物的反应的离子方程式 。
(3)抽滤的好处是 ,从“母液”中回收有机溶剂的方法是 。
(4)“粗品纯化”的操作为蒸馏水洗涤、 洗涤、干燥,其中干燥过程使用的设备最好选用 (填“常压干燥机”或“真空干燥机”)。
(5)有文献指出,若在“水浴加热”过程中投入适量的石灰石,则能同时提高产品的产率和纯度,请解释原因: 。
(6)若甘氨酸的投料量为300 kg,产出纯品346.8 kg,则产率为 。(甘氨酸的相对分子质量为75)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用CaSO4代替O2与燃料CO反应,既可提高燃烧效率,又能得到高纯CO2,是一种高效、清洁、经济的新型燃烧技术。反应①为主反应,反应②和③为副反应。
①1/4CaSO4(s)+CO(g) ![]() 1/4CaS(s)+CO2(g) H1
1/4CaS(s)+CO2(g) H1
②CaSO4(s)+CO(g) ![]() CaO(s)+CO2(g) +SO2(g) H2
CaO(s)+CO2(g) +SO2(g) H2
③CO(g) ![]() 1/2C(s)+1/2CO2(g) H3
1/2C(s)+1/2CO2(g) H3
则反应2CaSO4(s)+7CO(g) ![]() CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的H=
CaS(s)+CaO(s)+6CO2(g)+C(s) +SO2(g)的H=
(用H1、H2和H3表示)
(2)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g) ![]() CH3OCH3(g)+3H2O(g);ΔH
CH3OCH3(g)+3H2O(g);ΔH
①该反应平衡常数表达式为K= 。
②已知在某压强下,该反应在不同温度、不同投料比时,CO2的转化率如图所示。该反应的ΔH____(填“>”“<”或“=”)0。若温度不变,减小反应投料比[n(H2) /n(CO2)],则K将 (填“增大”“减小”或“不变”)。
③二甲醚燃料电池具有启动快,效率高等优点,若电解质为酸性,二甲醚燃料电池的负极反应为 。
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:
2SO2+2nCu+(n+1)O2+(2-2n) H2O=2nCuSO4+(2-2n) H2SO4
从环境保护的角度看,催化脱硫的意义为 。
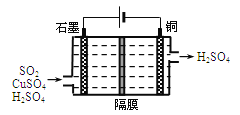
②利用下图所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的总的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成XH3、H2Z和HW共价化合物;Y与氧元素可组成Y2O和Y2O2的离子化合物。
(1)写出Y2O2的电子式:____ _,其中含有的化学键是___ _。
(2)用电子式表示Y2O的形成过程________ _______。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,稀溶浓氧化性最强的是_____(填化学式)。
(4)XH3、H2Z和HW三种化合物,其中一种与另外两种都能反应的是__________(填化学式)。
(5)由X、Y组成的化合物分子中.X、W原子的最外层均达到8电子稳定结构,该化合物遇水可生成一种具有漂白性的化合物,试写出反应的化学方程式_______________ ____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁子香酚可用作杀虫剂和防腐剂,其结构简式如图:。

(1)写出丁子香酚的分子式__________,其含氧官能团名称为__________。
(2)下列物质不能与丁子香酚发生反应的是______(填序号)。
a.NaOH溶液 b.NaHCO3溶液 c.Br2的四氯化碳溶液 d.乙醇
(3)丁子香酚的一种同分异构体:对甲基苯甲酸乙酯(E)是有机化工原料,用于合成药物的中间体。E的合成路线如下:

①指出化学反应类型:甲____ ______;乙_____ _____。
②写出反应丙的化学反应方程式:_________ _____________。
③写出符合下列条件的C的同分异构体:__________。(只答其中一种即可)
ⅰ含有苯环; ⅱ能够发生银镜反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com