
| A. | 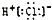 | B. | 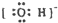 | C. | 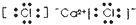 | D. | 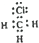 |
分析 A.氯化氢属于共价化合物;
B.氢氧根离子为阴离子,带1个单位负电荷,氧原子与氢原子共用1对电子;
C.CoCl2属于离子化合物;
D.CH3Cl为共价化合物,碳原子与3个氢原子各共用1对电子,与氯原子共用1对电子;
解答 解:A.氯化氢为共价化合物,氢原子与氯原子共用1对电子,电子式为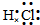 ,故A错误;
,故A错误;
B.氢氧根离子为阴离子,带1个单位负电荷,氧原子与氢原子共用1对电子,电子式为: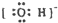 ,故B正确;
,故B正确;
C.CoCl2属于离子化合物,电子式为: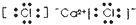 ,故C正确;
,故C正确;
D.CH3Cl为共价化合物,碳原子与3个氢原子各共用1对电子,与氯原子共用1对电子,电子式为: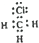 ,故D正确;
,故D正确;
故选:A.
点评 本题考查电子式的正误判断,题目难度不大,主要是考查学生对常见物质电子式的熟悉了解程度,明确物质中化学键的类型是解题的关键.


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 先关水龙头,拔下抽滤瓶上的橡皮管,再取下布氏漏斗 | |
| B. | 先取下布氏漏斗,再关上水龙头 | |
| C. | 先将沉淀和滤纸一起取出,再关上水龙头 | |
| D. | 先拔下抽滤瓶上的橡皮管,关上水龙头,再取下布氏漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | |
| B. | 混合气体的密度 | |
| C. | 当B、C、D三种物质,它们的物质的量nB:nC:nD=2:1:1 | |
| D. | 混合气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是银白色的柔软金属,密度都比水小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 碱金属单质都能与盐酸反应放出氢气 | |
| D. | 单质的熔、沸点随着原子序数的增加而升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①⑥ | C. | ④⑥ | D. | ⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 第二周期 | Li | Be | B | C | N | O | F |
| 电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | |
| 第三周期 | Na | Mg | Al | Si | P | S | Cl |
| 电负性值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 | |
| B. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 | |
| C. | 反应速率越大,则单位时间内生成物的产量就越大 | |
| D. | 在反应过程中,反应物浓度逐渐变小,所以用反应物表示的化学反应速率为负值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com