


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| 次序 | 稀盐酸(ml) | 剩余固体(g) |
| 1 | 先加入5.0 | 1.32 |
| 2 | 加入5.0 | 0.64 |
| 3 | 加入5.0 | 0.20 |
| 4 | 加入5.0 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、SO42-、H2SO3 |
| B、Na+、SiO32-、Cl-、NO3- |
| C、H+、Al3+、SO42-、NH4+ |
| D、Na+、S2-、H+、S2O32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
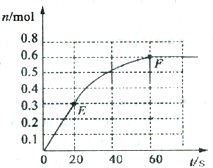 373K时,某1L恒容密闭容器中加入1molNH3,发生如下可逆反应2NH3(g)?N2(g)+3H2(g).其中物质H2的物质的量随时间变化如图所示.
373K时,某1L恒容密闭容器中加入1molNH3,发生如下可逆反应2NH3(g)?N2(g)+3H2(g).其中物质H2的物质的量随时间变化如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属单质与盐溶液的反应都是置换反应 |
| B、SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 |
| C、Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 |
| D、C、N、S三种单质直接与O2反应都能生成两种以上氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
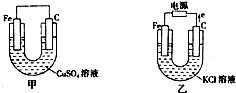 根据如图所提供的信息,在反应一段时间后:
根据如图所提供的信息,在反应一段时间后:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、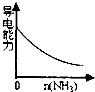 氨气通入硫酸溶液中 |
B、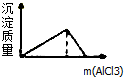 NaOH溶液中逐滴加入AlCl3溶液至过量 |
C、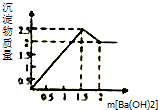 向1L1.0mol?L-1的明矾溶液中加入Ba(OH)2溶液 |
D、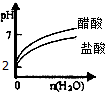 pH=2的盐酸和醋酸分别加水稀释 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com