
| A. | 8g | B. | 15.5g | C. | 11.7g | D. | 无法确定 |
分析 Na2O2、Na2O、Na2CO3、NaOH的混合物与盐酸恰好反应,所得溶液中溶质为NaCl,溶液蒸干所得固体为NaCl,根据氯原子守恒有n(NaCl)=n(HCl),根据m(溶质)=m(溶液)×w(溶质)计算m(HCl),进而计算n(NaCl),再根据m=nM计算NaCl的质量.
解答 解:Na2O2、Na2O、Na2CO3、NaOH的混合物与盐酸恰好反应,所得溶液中溶质为NaCl,溶液蒸干所得固体为NaCl,
根据氯原子守恒可得:n(NaCl)=n(HCl),
盐酸中氯化氢的质量为:m(HCl)=200g×3.65%=7.3g,
则:n(NaCl)=n(HCl)=$\frac{7.3g}{36.5g/mol}$=0.2mol,
所以最终得到NaCl的质量为:0.2mol×58.5g/mol=11.7g,
故选C.
点评 本题考查混合物的有关计算,题目难度不大,题目涉及反应过程比较多,但过程不复杂,侧重考查学生的解题方法技巧与思维能力,注意利用守恒思想进行解答.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 1:1 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
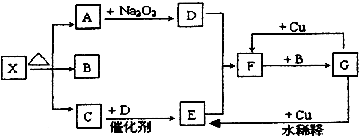
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Br-,I-,Cl-,S2- | B. | Br-,Cl-,I-,S2- | C. | Br-,Cl-,S2-,I- | D. | Cl-,I-,S2--,Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同体积,不同密度的N2和CO两种气体 | |
| B. | 相同密度的O2和O3两种气体 | |
| C. | 相同质量,不同密度的C2H4和C3H8两种气体 | |
| D. | 相同物质的量,不同体积的NH3和CH4两种气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ④ | B. | ④⑤ | C. | ①④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
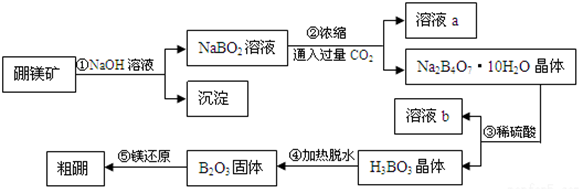
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
工业上常用铁质容器盛装冷浓硫酸.为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com