
【题目】下列说法中正确的是( )
A.C60气化和干冰升华克服的作用力相同
B.分子晶体在水溶液中一定能导电
C.氯化钠和氯化氢溶于水时,破坏的化学键都是离子键
D.用作高温结构陶瓷材料的Si3N4固体是分子晶体
科目:高中化学 来源: 题型:
【题目】欲配制480mL0.5mol·L-1的NaOH溶液,试回答下列问题。
(1)计算:需要NaOH固体的质量为___________。
(2)假定最终称量小烧杯的质量为____________(填“32.6g”或“32.61g”)。
在标尺(图)上画出游码位置(画“△”表示)。
![]()
(3)某学生实际配制的NaOH溶液的浓度为0.51mol·L-1,原因可能是________。
A.使用滤纸称量NaOH固体 |
B.容量瓶中原来存有少量水 |
C.溶解后的烧杯未经多次洗涤 |
D.用胶头滴管加水定容时俯视刻度 |
E.加水时超过刻度线,用胶头滴管吸出
F.转移溶液时未经冷却
(4)假设该同学成功配制了0.400mol·L-1的盐酸,他又用该盐酸中和含100 mL的NaOH溶液,则该同学需取________mL盐酸。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙;向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )
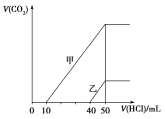
A.原NaOH溶液的物质的量浓度为0.5 mol·L-1
B.当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+===H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D.乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
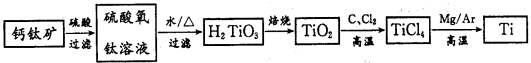
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为___________晶体。
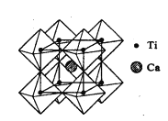
(2)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被____个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被____个氧离子包围。
(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:
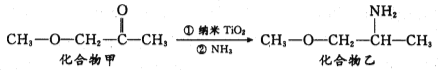
化合物甲中C原子的杂化方式为_______________;化合物乙的沸点明显高于化合物甲,主要原因是_______________________________。
II. 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(4)镍元素在元素周期表中的位置为 。
(5)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(6)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(7)Ni的氯化物与氨水反应可形成配合物[Ni(NH3)4]Cl2,2mol该配合物中含有σ键______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.NaCl(aq)![]() NaHCO3(s)
NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s)
B.CuCl2![]() Cu(OH)2
Cu(OH)2![]() Cu
Cu
C.Al ![]() NaAlO2(aq)
NaAlO2(aq) ![]() NaAlO2(s)
NaAlO2(s)
D.MgO(s)![]() Mg(NO3)2(aq)
Mg(NO3)2(aq) ![]() Mg(s)
Mg(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3H2O、NH4+、NH3扩散到水槽中),所得溶液的密度为ρgcm﹣3。下列说法正确的是( )
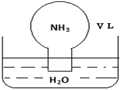
A.条件不足,不能计算所得溶液的物质的量浓度
B.所得溶液中,n(NH3H2O)+n(NH4+)+n(NH3)=![]() mol
mol
C.所得溶液的质量分数为![]() ρ
ρ
D.水最终不可能充满整个烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:
A.金刚石与石墨;
B.淀粉与纤维素;
C.氕与氘;
D.甲烷与戊烷;
E.葡萄糖与果糖
F.![]() 与
与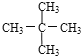
G.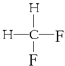 与
与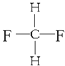
其中互为同位素 ;(填编号.下同),互为同系物的是 ,互为同分异构体的是 ,是同一种物质的是 .
(2)120℃,101kpa下,9ml由CO和C2H4组成的混合气体在足量的O2中完全燃烧后,恢复到原温度和压强.测得混合气体完全燃烧所消耗O2的体积与生成CO2的体积相等.请回答下列问题。
①等体积的CO和C2H4在相同条件下完全燃烧,生成CO2的体积比为 ;消耗O2的体积比为 .
②燃烧前混合气体中CO的体积为 , C2H4的体积为 .
(3)①化合物A的结构简式为: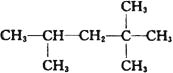 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
②篮烷分子的键线式如图所示,试回答:
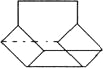
I写出篮烷分子的化学式____________;II篮烷分子的一氯取代物的种数为_______种。
(4)元素氮的一种液态氢化物叫肼,其分子中氮原子与氢原子个数比为1:2.肼﹣空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%﹣30%的KOH溶液.氮元素对应的燃烧产物为N2。该燃料电池的负极的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:

已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A 的化学名称为__________________,。
(2)B的结构简式为____________________。其核磁共振氢谱显示为______组峰,峰面积比为_______。
(3)由C生成D的反应类型为_____________。
(4)由D生成E的化学方程式为__________________________________________________________。
(5)G中的官能团有__________、__________、__________。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有___________种。(不含立体结构)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com