
三草酸合铁酸钾晶体[K3Fe(C2O4)3•xH2O]是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组实验步骤为:(1)称量9.820 g三草酸合铁酸钾晶体,配制成250 mL溶液。(2)取所配溶液25.00 mL于锥形瓶中,滴加酸性KMnO4溶液至C2O42-全部转化成CO2,同时MnO4-被转化成Mn2+,恰好消耗0. 1000 mol/L KMnO4溶液24.00 mL。[K3Fe(C2O4)3的相对分子质量为437] 下列说法正确的是
A.步骤(2)中KMnO4表现还原性
B.配制三草酸合铁酸钾溶液玻璃仪器只需烧杯和玻璃棒
C.样品中结晶水的物质的量为0.03 mol
D.该晶体的化学式为K3Fe(C2O4)3•3H2O
D
【解析】
试题分析:A、同时MnO4-被转化成Mn2+,锰元素化合价由+7→+2,化合价降低被还原,作氧化剂,故A错误;B、需要配制成250mL溶液,必须使用到250容量瓶和胶头滴管,故B错误; C、高锰酸钾得到电子等于C2O42-失去的电子,n得=0.1000mol/L×0.024L×(7-2)=0.012mol;C2O42-全部转化成CO2,化合价变化+3→+4,根据电子守恒 n(C2O42-)=0.012mol/ (2-1)×2=0.006mol;250mL原溶液C2O42-的物质的量为0.006mol×10=0.06mol,故n[K3Fe(C2O4)3]=0.06mol×1/3=0.02mol,9.820g三草酸合铁酸钾晶体中结晶水的质量为:9.820-437×0.02=1.08(g),故n(H2O)=1.08g/18g.mol−1=0.06mol,故C错误;D、根据C项计算结果,0.02molK3Fe(C2O4)3中还有0.06molH2O,结晶水数目为3,故该晶体的化学式为K3Fe(C2O4)3•3H2O,故D正确;故选D.
考点:中和滴定;探究物质的组成或测量物质的含量


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
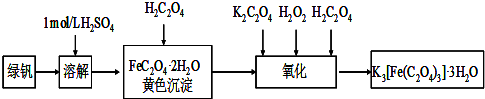
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
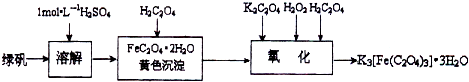
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
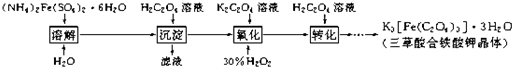
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
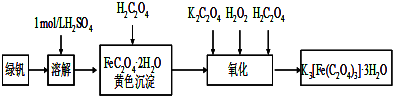
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com