
| A. | 84 g NaHCO3晶体中含有NA个CO32- | |
| B. | 室温下,14.0 g乙烯和丁烯的混合气体中含有C-H键数目为2.0NA | |
| C. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2NA | |
| D. | 78 g Na2O2与足量的CO2反应,电子转移个数为2NA |
分析 A、NaHCO3晶体中无CO32-;
B、乙烯和丁烯的最简式为CH2;
C、粗铜中含有还原性强于铜的杂质铁、锌,电解过程中优先放电;
D、求出Na2O2的物质的量,然后根据过氧化钠与二氧化碳的反应为歧化反应来分析.
解答 解:A、NaHCO3晶体中为Na+和HCO3-,无CO32-,故A错误;
B、乙烯和丁烯的最简式为CH2,故14g混合气体中含有的CH2的n=$\frac{14g}{14g/mol}$=1mol,故含有的C-H键的物质的量为2mol,故个数为2NA个,故B正确;
C、电解精炼铜时,阳极粗铜中含有活泼性较强的铁、先等杂质,电解时铁、锌杂质先放电,且铁摩尔质量小于铜的64g/mol,锌的摩尔质量大于铜的摩尔质量,所以阳极减少6.4g,转移的电子的物质的量不一定为0.2mol,故C错误;
D、78gNa2O2的物质的量为1mol,而过氧化钠与二氧化碳的反应为歧化反应,1mol过氧化钠转移1mol电子,即NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
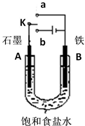
| A. | 若开始时开关K与a连接,其反应与铁的吸氧腐蚀类似 | |
| B. | 若开始时开关K与b连接,其原理类似于钢铁防护中外加电流的阴极保护法 | |
| C. | 若开始时开关K与b连接,则标准状况下B极产生2.24 L气体,转移电子0.2 mol | |
| D. | 若开始时开关K与b连接,则反应一段时间后加适量盐酸可恢复到电解前电解质相同的状态(质量和浓度均相同) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 最新的数据显示,北京雾霾颗粒中机动车尾气占22.2%,燃煤占16.7%,扬尘占16.3%,工业占15.7%.据分析六大主要雾霾贡献源如图所示.下列措施不可能改善空气质量的是( )
最新的数据显示,北京雾霾颗粒中机动车尾气占22.2%,燃煤占16.7%,扬尘占16.3%,工业占15.7%.据分析六大主要雾霾贡献源如图所示.下列措施不可能改善空气质量的是( )| A. | 应用高效洁净的能源转换技术,在大型燃煤锅炉上安装低氮燃烧器,采用烟气脱硝技术 | |
| B. | 不放烟花焰火,加强道路扬尘污染控制,强化路面保洁,洒水防尘 | |
| C. | 在炼油厂.钢铁厂.发电厂等,推广和使用脱硫技术,降低硫氧化物的排放 | |
| D. | 研究采煤.采油新技术,增加汽油.柴油等能源的供应量,提倡以汽车代步的现代消费与生活理念 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C7H8O,且属于芳香族化合物的同分异构体只有4种 | |
| B. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物最多有6种 | |
| C. | 丙烷的一氯代物有2种,丙烷的二氯代物有4种 | |
| D. | 联苯(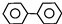 )的一氯代物有3种,二氯代物有12种 )的一氯代物有3种,二氯代物有12种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
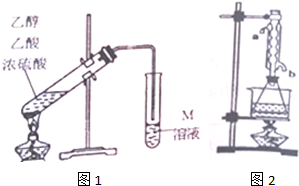
| 相对分子质量 | 沸点(℃) | |
| 乙醇 | 46 | 78.5 |
| 乙酸 | 60 | 117.9 |
| 乙酸乙酯 | 88 | 77.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
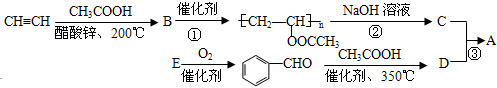
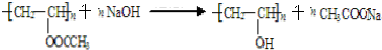 ;反应类型是取代反应.
;反应类型是取代反应. .
.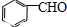 能发生银镜反应,该反应的化学方程式是
能发生银镜反应,该反应的化学方程式是 .
.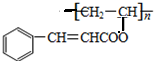 ,关于A的性质下列说法正确的是acd(填字母).
,关于A的性质下列说法正确的是acd(填字母).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com