
| m |
| n |
| 1000ρω |
| M |
| 16g |
| 0.25mol |
| 1000×1.19×36.5% |
| 36.5 |
| 33.6L |
| 22.4L/mol |
| 45g |
| 18g/mol |
| 1 |
| 4 |
| 1.204×1024 |
| 6.02×1023 |


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
| A、反应容器的压强不随时间而变化 |
| B、A气体和B气体的生成速率相等 |
| C、A气体和C气体的生成速率相等 |
| D、反应混合气体的密度不随时间而变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
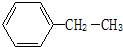
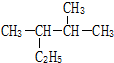
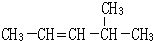
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验步骤(不要求写具体操作过程) | 预期现象和结论 |
| ①测定甲同学所用Fe(N3O)3溶液的pH ② … |
若银镜消失,假设2成立.若银镜不消失,假设2不成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 按要求问答下列问题
按要求问答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
| 太阳光 |

| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、和浓H2SO4共热至170℃时,键②和⑤断裂 |
| B、和乙酸共热发生酯化反应时,键②断裂 |
| C、在铜催化下和氧气反应时,键①和③断裂 |
| D、和氢卤酸共热时键②断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的O4和O2含有相同数目的原子 |
| B、O4是一种化合物 |
| C、等物质的量的O4和O2,前者所含的分子数多 |
| D、O4的摩尔质量是64g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com