
| A. | 放电时铅蓄电池负极电池反应 PbO2+4H++SO42-+2e-═PbSO4+2H2O | |
| B. | 充电时蓄电池阴极电极反应 PbSO4+2e-═Pb+SO42- | |
| C. | 用铅蓄电池来电解CuSO4溶液,要生成1.6g Cu,则该电池内部要消耗0.025mol H2SO4 | |
| D. | 铅蓄电池充电时,若要使3.03kg PbSO4转变为Pb和PbO2,则需要通过20mol电子 |
分析 放电时负极反应式为:Pb+SO42--2e-=PbSO4,正极反应式为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,电池充电时,阳极上的反应是放电时的正极反应的逆过程,阴极上的反应是放电时负极反应的逆过程,根据电极反应式结合电子守恒来解答.
解答 解:A.放电时,负极失去电子,则放电时铅蓄电池负极的电极反应为Pb+SO42--2e-=PbSO4,故A错误;
B.充电时,负极与阴极相连,则阴极的电极反应为PbSO4+2e-=Pb+SO42-,故B正确;
C.用铅蓄电池来电解CuSO4溶液,由电子守恒可知,2H2SO4~2e-~Cu,则生成3.2克Cu,消耗硫酸为$\frac{3.2g}{64g/mol}$×2=0.1mol,故C错误;
D.由2PbSO4~2e-可知,使3.03千克PbSO4转变为Pb和PbO2,转移电子为:$\frac{3030g}{303g/mol}$=10mol,故D错误;
故选B.
点评 本题考查铅蓄电池,为高频考点,题目难度中等,注意原电池和电解池的分析,明确工作原理及电子守恒是解答本题的关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl- | |
| B. | 实验已经证明,氯水是可以导电的,所以氯水是电解质 | |
| C. | 某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水 | |
| D. | 胶体与其它分散系的本质区别在于胶体具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石晶体中的最小碳原子环由6个碳原子构成 | |
| B. | SO3晶体属于原子晶体 | |
| C. | 1molSiO2晶体中含有2molSi-O键 | |
| D. | 金刚石化学性质稳定,即使高温下也不会和O2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol冰醋酸和1mol乙醇经催化加热反应可生成H2O分子数为NA | |
| B. | 常温常压下,将15g NO和8g O2混合,所得混合气体分子总数小于0.5NA | |
| C. | 标准状况下,2.24 L的CCl4中含有的C-Cl键数为0.4NA | |
| D. | 6.8g熔融态KHSO4中含有0.1NA个阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若8>m>3,则X必定为主族元素 | |
| B. | 若Y的气态氢化物化学式为YHn,且b<4,则该氢化物为极性分子 | |
| C. | 若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X | |
| D. | 若a=b=3,8>m>n>b,则元素非金属性:X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
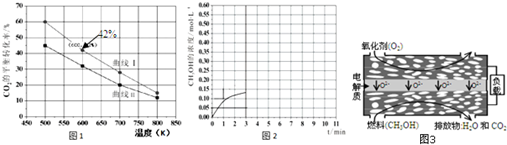
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干燥的Cl2和氯水均能使鲜花褪色 | |
| B. | SiO2具有导电性,可用于制造半导体材料 | |
| C. | 某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ | |
| D. | Fe2+、SO2都能使酸性高锰酸钾溶液褪色,前者表现出还原性后者表现出漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com