
【题目】宇宙飞船上使用的氢氧燃料电池是一种新型化学电池,其结构如图所示,A、B是多孔性碳制成的两个电极。
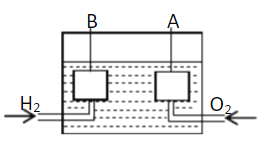
(1)该燃料电池的正极是 (填“A”或“B”),若电解质溶液为KOH溶液,则负极的电极反应式为 ;一段时间后,溶液的pH会 (填“变大”“变小”或“不变”)。
(2)若电解质溶液为硫酸,则正极的反应式为 。
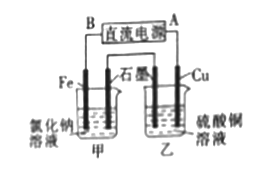
(3)若用该氢氧燃料电池作电源电解氯化钠溶液和硫酸铜溶液,装置如图所示,则铁电极上产生的气体为 (填化学式);一段时间后,铜电极的质量减少6.4g,则甲池中石墨电极上产生气体的物质的量为 。
【答案】(1)A;H2+2OH—-2e-=2H2O;变小
(2)O2+4H++4e-=2H2O
(3)H2;0.1mol
【解析】
试题分析:(1)氢氧燃料电池中,通入氢气的一极为电源的负极,通入氧气的一极为原电池的正极,该燃料电池的正极是A;由于电解质溶液呈碱性,则负极电极反应式为2H2-4e-+4OH-=4H2O;一段时间后,水的质量增大,碱溶液浓度减小,pH会减小;(2)若电解质溶液为硫酸,则正极的反应式为O2+4H++4e-=2H2O;(3)铁与负极相连,铁做阴极发生还原反应,电极反应为![]() ,铁电极上产生的气体为H2;,铜电极连接电源的正极,铜为阳极,电极反应为
,铁电极上产生的气体为H2;,铜电极连接电源的正极,铜为阳极,电极反应为![]() ,质量减少6.4g,转移电子0.2mol,甲池中石墨电极上的反应为
,质量减少6.4g,转移电子0.2mol,甲池中石墨电极上的反应为![]() ,根据电子守恒,产生气体的物质的量为0.1mol。
,根据电子守恒,产生气体的物质的量为0.1mol。


科目:高中化学 来源: 题型:
【题目】可逆反应 N2(g)+3H2(g)![]() 2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
2NH3(g),在500℃时,将2molN2和2molH2冲入容积为10L的密闭容器中进行反应,达到平衡时,NH3不可能达到的浓度是( )
A.0.01mol·L-1B.0.02mol·L-1
C.0.05mol·L-1D.0.15mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-选修3:物质结构与性质】张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)N、P、As原子的第一电离能由大到小的顺序为_______;As原子的核外电子排布式为______________。
(2)NH3的沸点比PH3_____(填“高"或“低”),原因是_____________。
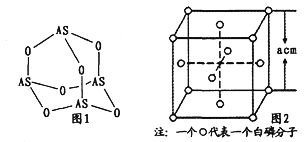
(3)Na3AsO4中含有的化学键类型包括_______;AsO43-的空间构型为_______,As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是_________。
(4)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子)。己知晶胞的边长为acm,阿伏加德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为______,该晶体的密度为___g·cm-3(用含NA、a的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种利用钛铁矿制备Li4Ti5O12的工艺流程如图:

已知:钛铁矿的主要成分是FeTiO3(可表示为FeO·TiO2),还含有少量的MgO和SiO2等杂质。
回答下列问题:
(1)酸浸时,要提高铁的浸出率可采取的措施是___(写出一条即可)。
(2)酸浸后的滤液①中钛主要以TiOCl42-形式存在,则其水解生成TiO2·xH2O的离子方程式为___,加热水的目的是___。
(3)TiO2·xH2O沉淀与双氧水、氨水反应时,应将温度控制在50℃左右的原因是___。
(4)若将滤液②加热至一定温度后,再加入双氧水和磷酸,恰好使Mg2+沉淀完全[溶液中c(Mg2+)降至1.0×10-5mol·L-1],此时溶液中![]() =___。已知:此温度下,FePO4、Mg3(PO4)2的溶度积常数分别为1.5×10-21、1.0×10-23。
=___。已知:此温度下,FePO4、Mg3(PO4)2的溶度积常数分别为1.5×10-21、1.0×10-23。
(5)高温煅烧时发生反应的化学反应方程式为___。
(6)某可充电的锂离子电池以Li4Ti5O12为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质。放电时的电池反应为LixC+Li4Ti5O12=Li(x-5)C+Li9Ti5O12,则充电时阴极电极反应式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《X-MOL》报道:RobertPipes等设计的添加PDS(![]() )的Li-CO2电池,正极物质转化原理如图所示。下列说法错误的是( )
)的Li-CO2电池,正极物质转化原理如图所示。下列说法错误的是( )

A.PDS起增强导电性作用
B.负极反应式为Li-e-=Li+
C.电池总反应为4Li+3CO2=2Li2CO3+C
D.正极上发生的反应之一为![]() +2CO2+2e-=2
+2CO2+2e-=2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
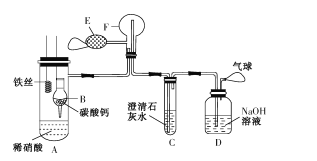
【题目】为了证明铁与稀硝酸反应产生一氧化氮,某校兴趣小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去)。B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;F为一个空的蒸馏烧瓶;E是用于鼓入空气的双连打气球。
回答下列问题:
(l)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,一段时间后,C中澄清石灰水____(填现象)时,将B装置上提,使之与稀硝酸分离。
(2)将A中铁丝放入稀硝酸中,装置A中产生________(填“无色”或“红棕色”)气体。用E向F中鼓入空气后,烧瓶F内发生反应的化学方程式为 ___, 一段时间后,C中的现象为____。
(3)若反应后向A中溶液滴加KSCN溶液,溶液不变红色,则铁丝与稀硝酸反应的离子方程式为________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1![]() 二元弱酸
二元弱酸![]() 溶液的pH,溶液中的
溶液的pH,溶液中的![]() 、
、![]() 、
、![]() 的物质的量分数
的物质的量分数![]() 随pH的变化如图所示[已知
随pH的变化如图所示[已知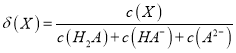 ]。
]。
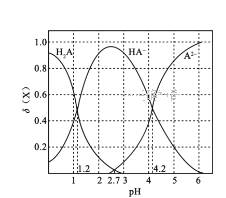
下列叙述错误的是( )
A. pH=1.2时, ![]()
B. ![]()
C. pH=2.7时, ![]()
D. pH=4.2时, ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化钛在一定波长光的照射下,可有效降解甲醛、苯等有机物,效果持久,且自身对人体无害。某课题组研究了溶液的酸碱性对TiO2光催化染料R降解反应的影响,结果如图所示。下列判断正确的是

A. 在0~50 min之间,R的降解百分率pH=2大于pH=7
B. 溶液酸性越强,R的降解速率越大
C. R的起始浓度不同,无法判断溶液的酸碱性对R的降解速率的影响
D. 在20~25 min之间,pH=10时R的降解速率为0.04 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤、石油、淀粉都是基础的化工原料,它们之间存在如下关系(部分产物和反应条件未标出)。B为相对分子质量为28的烃;E为淀粉水解的最终产物;F分子中含有一个甲基和一个羧基,lmolF与足量的钠反应能生成标况下22.4LH2;D物质中也含有羧基。

回答下列各题:
(1)若A为煤焦油,则从A中分离出苯的方法是__________,工业上通过石油的________制B物质.
(2)C为乙苯,则苯和B生成C的反应类型是____________, C的结构简式是____________.
(3)写出B制备聚乙烯的反应方程式_____________________________________________.
(4)写出D与F转化为G的反应方程式________________________________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com