

回答下列问题:
(1)装置I中,仪器a的名称叫_________。
(2)当Cl2气流通过一段时间后,装置Ⅱ中溶液的pH_________(填“>”“<”或“=”)7。
(3)当有少量Cl2气流通过后,装置Ⅲ中反应的离子方程式为__________________。
(4)当Cl2气流持续通过时,装置Ⅳ中干燥的有色布条能否褪色?_________。
(5)装置V的作用是____________________________。
科目:高中化学 来源:2012-2013学年重庆市重庆一中高一4月月考化学试卷(带解析) 题型:单选题
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,正确的是
A.用电子式表示溴化氢的形成过程为: |
B.海水中Br-的电子式为: |
| C.海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl |
D.氯离子的结构示意图为: |
查看答案和解析>>
科目:高中化学 来源:2014届河南省高三上学期期中考试化学试卷(解析版) 题型:填空题
氯、溴、碘、钠、镁、锰、锂、铀等元素在海洋中被富集。海洋开发利用和维权是国家战略。
(1)以上元素在海水中的存在形态是___________(选填①游离态②化合态③不确定)
(2)以下变化属于化学变化的是__________________________:
① 发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
(3)由氯气和晒盐后的卤水制取液溴的离子方程式______________________________;由石灰乳和卤水沉淀出镁元素的离子方程式_____________________________________;由海带灰可浸出KI,由某种矿盐可浸出KIO3,二者在盐酸中反应可生成碘单质,反应的离子方程式__________________________________。
(4)工业由氯化钠制取金属钠的化学方程式为____________________________;工业制镁采用电解熔融氯化镁,不采用电解熔融氧化镁的原因是_______________________
(5)海底富集多种矿物结核,锰结核是其中的一种。锰结核中主要含有MnO2和Fe2O3。一种质量比约为m(Mn):m(Fe)=55:448的合金钢(其它元素略),具有抗御激烈冲击和磨损的能力,可做航母甲板等。欲通过铝热反应炼得这样的合金,MnO2、Fe2O3、Al的投料比(按物质的量之比)约为_______________。
查看答案和解析>>
科目:高中化学 来源:2015届重庆市高一4月月考化学试卷(解析版) 题型:选择题
在海水的综合利用中,海水提溴工业是一个重要组成部分,其中一种提溴的工艺是在预先浓缩并酸化的海水中,通入足量氯气,然后使生成的溴与吸收剂SO2反应转化为氢溴酸以达到富集溴元素的目的。在有关上述工艺流程的以下化学用语中,正确的是
A.用电子式表示溴化氢的形成过程为: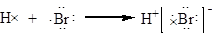
B.海水中Br-的电子式为: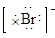
C.海水中通入氯气时发生反应的离子方程式为:2NaBr+Cl2=Br2+2NaCl
D.氯离子的结构示意图为: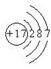
查看答案和解析>>
科目:高中化学 来源:0127 会考题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com