
【题目】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:

相关反应的热化学方程式为:
反应I:SO2(g) + I2(g) + 2H2O(l) === 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1
反应II:H2SO4(aq) === SO2(g) + H2O(l) + ![]() O2(g) ΔH2 = +327 kJ·mol-1
O2(g) ΔH2 = +327 kJ·mol-1
反应III:2HI(aq) === H2(g) + I2(g) ΔH3 = +172 kJ·mol-1
下列说法不正确的是:
A. 该过程实现了太阳能到化学能的转化
B. SO2和I2对总反应起到了催化剂的作用
C. 总反应的热化学方程式为:2H2O(l) === 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1
D. 该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变
 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】某探究小组利用丙酮的溴代反应(CH3COCH3+Br2![]() CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率 v(Br2) 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率 v(Br2) 通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
实验序号 | 初始浓度c/mol·L-1 | 溴颜色消失所需时间t/s | ||
CH3COCH3 | HCl | Br2 | ||
① | 0.80 | 0.20 | 0.0010 | 290 |
② | 1.60 | 0.20 | 0.0010 | 145 |
③ | 0.80 | 0.40 | 0.0010 | 145 |
④ | 0.80 | 0.20 | 0.0020 | 580 |
分析实验数据所得出的结论不正确的是( )
A.增大c(CH3COCH3),v(Br2)增大
B.实验②和③的v(Br2)相等
C.增大c(HCl),v(Br2)增大
D.增大c(Br2),v(Br2)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯酸钾熔化,粒子间克服了__的作用力;二氧化硅熔化,粒子间克服了__的作用力;碘的升华,粒子间克服了__的作用力.三种晶体的熔点由高到低的顺序是__.
(2)下列六种晶体:①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,它们的熔点从低到高的顺序为__(填序号).
(3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有__,由非极性键形成的非极性分子有__,能形成分子晶体的物质是__,含有氢键的晶体的化学式是__,属于离子晶体的是__,属于原子晶体的是__,五种物质的熔点由高到低的顺序是__.
(4)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__.
(5)图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
A.__;B.__;C.__;D.__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 天然植物油常温下一般呈液态,难溶于水,熔点、沸点比动物脂肪低
B. 葡萄糖有醛基,果糖不含醛基,故二者可用银镜反应鉴别
C. 若两种二肽互为同分异构体,则二者的水解产物可能相同,也可能不同
D. 含5个碳原子的有机物,每个分子中最多可形成4个C—C单键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于苯乙烯(![]() )的说法中不正确的是( )
)的说法中不正确的是( )
A. 分子中所有原子可能在同一个平面
B. 在一定条件下,1mol 苯乙烯最多消耗4mol H2
C. 和H2充分反应后的产物一氯代物有5种
D. 苯乙烯可发生还原反应、氧化反应、加成反应、加聚反应、取代反应等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.已知:![]()
烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3:4,与A相关的反应如下:
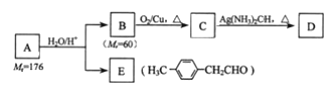
请回答下列问题:
(1)A的分子式为__,B的名称是__;
(2)写出C→D反应的化学方程式:__;
(3)链烃M的相对分子质量比B多24,分子中所有碳原子均在同一平面上,其结构简式是__;
Ⅱ.由E转化为对甲基苯乙炔(![]() )的一条路线如下:
)的一条路线如下:

(4)①反应中所加试剂是__; ③的反应类型是__;
(5)写出G的结构简式:__;
(6)写出两种同时符合下列条件的E的同分异构体的结构简式:__。
①属于芳香醛;
②苯环上有两种不同环境的氢原子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在酸性溶液中能大量共存且溶液呈无色透明的是
A.K+、Na+、SiO32-、Br-B.Na+、K+、CH3COO-、NO3-
C.K+、Cl-、Fe3+、SO42-D.Mg2+、Al3+、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛工厂TiCl4烟尘中含有大量的ScCl3、MgCl2及SiO2小颗粒等物质,某研究所利用上述烟尘回收Sc2O3,并制备钛白粉(TiO2),其工艺流程如下所示:

(1)酸浸过程中,HCl的作用是_______________________。
(2)已知Sc3++3HTBP![]() Sc(TBP)3+3H+,则上述洗脱剂最好选择___________(选填“酸性”、“碱性”或“中性”)溶液。在实验室模拟完成上述操作Ⅰ和操作Ⅱ所涉及的玻璃仪器有______________。
Sc(TBP)3+3H+,则上述洗脱剂最好选择___________(选填“酸性”、“碱性”或“中性”)溶液。在实验室模拟完成上述操作Ⅰ和操作Ⅱ所涉及的玻璃仪器有______________。
(3)草酸“沉钪”得到草酸钪的化学反应类型为____________________________。
(4)在空气中灼烧草酸钪即可得到氧化钪(Sc2O3),其化学反应方程式为__________________________。
(5)“水相”的主要离子有TiOCl42-、H+、Cl- 及________,写出加入大量的水并加热发生的相关离子反应方程式__________________________。
(6)钛的冶炼新法是剑桥电解法(如右图)。
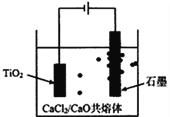
以含少量CaCl2的CaO熔融物作为介质,电解时。在阴极生成的Ca进一步还原TiO2得钛。写出阳极电极主要反应方程式:__________________________;利用中学所学知识可以预测CaCl2的作用包含增强导电性、___________;F=96500C/mol,当I=0.5A,通电80分钟,理论上获得Ti的质量为__________g(计算表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com