
NH3及其盐都是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反 应发生、气体收集和尾气处理装置依次为_____________。
应发生、气体收集和尾气处理装置依次为_____________。
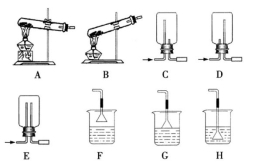
(2)按下图装置进行NH3性质实验。
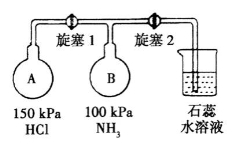
①先打开旋塞1,B瓶中的现象是_______________,原因是____________,稳定后,关闭旋塞1。
②再打开旋塞2,B瓶中的现象是_____________。
(3)设计实验,探究某一种 因素对溶液中NH4Cl水解程度的影响。
因素对溶液中NH4Cl水解程度的影响。
限制试剂与仪器:固体NH4Cl、蒸馏水、100mL容量瓶、烧杯、胶头滴管、玻璃棒、药匙、天平、PH计、温度计、恒温水浴槽(可控制温度)
①实验目的:探究对溶液中NH4Cl水解程度的影响。
②设计实验方案,拟定实验表格,完整体现实验方案(列出能直接读取数据的相关物理量及需拟定的数据,数据用字母表示;表中V(溶液)表示所配制溶液的体积)。
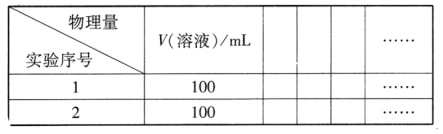
③按实验序号I所拟数据进行实验,若读取的待测物理 量的数值为Y,则NH4Cl水解反应得平衡转化率为______________ (只列出算式,忽略水自身电离的影响)。
量的数值为Y,则NH4Cl水解反应得平衡转化率为______________ (只列出算式,忽略水自身电离的影响)。
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:2016-2017学年陕西省高二上期中化学卷(解析版) 题型:选择题
下列说法中,正确的是( )
A.强电解质溶液一定比弱电解质溶液的导电性强
B.强电解质的水溶液中不存在分子
C.SO2和乙醇均属共价化合物,在水中都不能电离,均属非电解质
D.不同的弱电解质只要物质的量浓度相同,电离程度也相同
查看答案和解析>>
科目:高中化学 来源:2017届山东省日照市高三上学期期中化学试卷(解析版) 题型:选择题
下列判断合理的是( )
A.Na2O2、Fe2O3和A12O3属于碱性氧化物
B.蔗糖、硫酸钠和硫酸钡分别属于非电解质、强电解质和弱电解质
C.根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液
D.根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第三次周考化学卷(解析版) 题型:填空题
氨的化合物合成、应用及氨的固定一直是科学研究的热点。
(1)以CO2与NH3为原料合成化肥尿素的主要反应如下:
①2NH3(g)+CO2(g)=NH2CO2NH4(s);ΔH=-159.47kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g);ΔH=akJ·mol-1
③2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g);ΔH=-86.98kJ·mol-1
则a为______________。
(2)反应2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
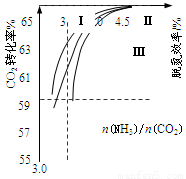
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值分别为:
A.0.6~0.7 B.1~1.1 C.1.5~1.61
生产中应选用水碳比的数值为 ___________(选填序号)。
②生产中氨碳比宜控制在4.0左右,而不是4.5的原因可能是 。
(3)尿素可用于湿法烟气脱氮工艺,其反应原理为:
NO+NO2+H2O=2HNO2;2HNO2+CO(NH2)2=2N2↑+CO2↑+3H2O。
①当烟气中NO、NO2按上述反应中系数比时脱氮效果最佳。若烟气中V(NO)∶V(NO2)=5∶1时,可通入一定量的空气,同温同压下,V(空气)∶V(NO)= (空气中氧气的体积含量大约为20%)。
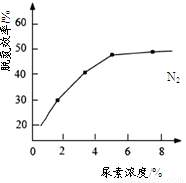
②下图是尿素含量对脱氮效率的影响,从经济因素上考虑,一般选择尿素浓度约为_________%。
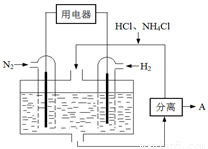
(4)下图表示使用新型电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制造出既能提供能量,同时又能实现氮固定的新型燃料电池。请写出该电池的正极反应式___________________。生产中可分离出的物质A的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第三次周考化学卷(解析版) 题型:选择题
分枝酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是
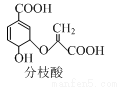
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1mol分枝酸最多可与3molNaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上11月月考化学卷(解析版) 题型:选择题
下列有关溶液组成的描 述合理的是
述合理的是
A.无色溶液中可能大量存在Al3+、NH4+、Cl?、S 2-
B.酸性溶液中可能大量存在Na+、ClO?、SO42-、I?
C.弱碱性溶液中可能大量存在Na+、K+、Cl?、HCO3?
D.中性溶液中可能大量存在Fe3+、K+、Cl?、SO42-
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上模拟四化学卷(解析版) 题型:填空题
二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。与Cl2相比, ClO2不但具有更显著的杀菌能力, 而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2 的制备方法中, 有下列两种常用制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为__________________,其中方法二制备的ClO2 更适合用于饮用水的消毒, 其主要原因是 。
(2)我国最近成功研制出制取ClO2 的新方法, 其反应的微观过程如图甲所示:
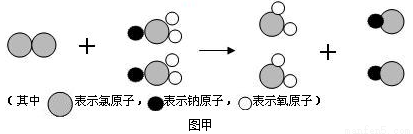
该反应的化学方程式为 。
(3)消毒时, ClO2对污水中Fe2+、Mn2+、S2-和CN— 等有明显的去除效果.某工厂污水中含CN—,现用ClO2将CN—氧化,生成两种无毒气体,其离子反应方程式为 。
(4)自来水厂用ClO2 处理后的水中, 要求ClO2 的浓度在0. 1~0. 8mg/L之间。碘量法可以检测水中ClO2 的浓度,步骤如下:
Ⅰ. 取一定体积的水样用氢氧化钠溶液调至中性, 然后加入一定量的碘化钾, 并加入淀粉溶液, 溶液变蓝。
Ⅱ. 加入一定量的Na2S2O3 溶液。(已知: 2S2O32- +I2 =S4O62- +2I - )
Ⅲ. 重复上述操作2~3次。
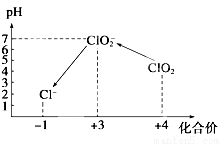
操作时, 不同pH环境中粒子种类如上图所示:
请回答:
①操作Ⅰ中反应的离子方程式是 ;
②确定操作Ⅱ恰好完全反应的现象是 ;
③若水样的体积为1. 0 L, 在操作Ⅱ时消耗了1. 0×10 -3 mol/L的Na 2 S 2 O 3 溶液10 mL, 则水样中ClO2 的浓度是 mg/L。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上12月月考化学试卷(解析版) 题型:选择题
现有易溶强电解质的混合溶液10L,其中可能含有K+、Ba2+、Na+、NH4+、Cl-、SO42-、AlO2-、OH-中的几种,向其中通入CO2气体,产生沉淀的量与通入CO2的量之间的关系如下明所示,下列说法正确的是
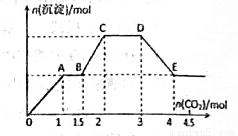
A.该溶液中能确定存在的离子是Ba2+、AlO2-、NH4+
B.肯定不存在的离子是SO42-、OH-
C.若不能确定的离子中至少还存在着一种阳离子,则该离子的最小浓度为0.2 mol/L
D.OA段反应的离子方程式:2 AlO2-+ CO2+3H2O=2Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二12月月考化学试卷(解析版) 题型:填空题
(1)某温度时,水的离子积Kw=1×10-13,则该温度____________(填“大于”、“小于”或“等于”)25℃,其理由是_____________________。在此温度下,某溶液中由水电离出来的H+浓度为1×10-10mol/L,则该溶液的pH可能为 。
(2)若温度为25℃时,体积为Va、pH=a的H2SO4与体积为Vb、pH=b的NaOH混合,恰好中和。此溶液中各种离子的浓度由大到小的排列顺序是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com