

分析 根据题意可知,用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成,用双氧水产生氧气,用纯氧气将CxHyOzNp氧化成二氧化碳、水和氮气,用氧化铜将未完全氧化的碳元素氧化成二氧化碳,用浓硫酸吸收水,用碱石灰吸收二氧化碳,用铜网吸收未反应的氧气,用排水量气法测得氮气的体积,为了准确测得各成分的质量,实验开始先用氧气将装置中的空气排尽,同时应按先吸收水,再吸收二氧化碳,再除氧气,最后测氮气的体积,根据元素守恒可计算出CxHyOzNp的组成,以此解答该题.
解答 解:根据题意可知,用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成,用双氧水产生氧气,用纯氧气将CxHyOzNp氧化成二氧化碳、水和氮气,用氧化铜将未完全氧化的碳元素氧化成二氧化碳,用浓硫酸吸收水,用碱石灰吸收二氧化碳,用铜网吸收未反应的氧气,用排水量气法测得氮气的体积,为了准确测得各成分的质量,实验开始先用氧气将装置中的空气排尽,同时应按先吸收水,再吸收二氧化碳,再除氧气,最后测氮气的体积,根据元素守恒可计算出CxHyOzNp的组成,
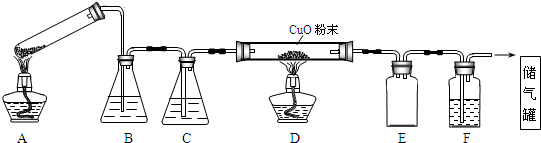
(1)空气中的氮气会产生干扰,首先要通入一段时间的氧气,将装置中的N2排净,之后,则需关闭止水夹a,打开b,
故答案为:排除装置内空气,避免它对实验造成干扰;a;b;
(2)氨基酸和氧气的反应,以及铜网和氧气的反应都需要加热,应先点燃D处的酒精灯,吸收未反应的氧气,保证最终收集的气体为N2,
故答案为:A、D;A;
(3)氨基酸和氧气反应的化学方程式是:CxHyOxNp+(x+$\frac{y}{4}$-$\frac{z}{2}$)O2$\stackrel{点燃}{→}$ xCO2+$\frac{y}{2}$H2O+$\frac{p}{2}$N2,
故答案为:CxHyOxNp+(x+$\frac{y}{4}$-$\frac{z}{2}$)O2$\stackrel{点燃}{→}$ xCO2+$\frac{y}{2}$H2O+$\frac{p}{2}$N2;
(4)根据以上分析可知,铜网的作用是吸收未反应的O2,保证最终收集到的气体是反应生成的N2,
故答案为:吸收未反应的氧气;
(5)为将N2所排水的体积测准,反应前应将连接E和F装置的玻璃导管中充满水,原因是N2将瓶E内的水首先排至导管中,其体积难以测定,为保证实验的精确度,使量筒内水的体积正好等于N2的体积,
故答案为:水;N2将瓶E内的水首先排至导管中,其体积难以测定,为保证实验的精确度,使量筒内水的体积正好等于N2的体积;
(6)读数时必须保证压强相同,所以注意事项是①量筒中的液面应与广口瓶中的液面相持平;其次②视线应与刻度线和凹液面最低点相切,
故答案为:视线与量筒内水的凹液面相平;移动量筒使其液面与瓶E内的水面在同一水平上;
(7)根据上面的分析可知,为了确定此氨基酸的分子式,除了准确测量N2的体积外,还需得到氨基酸的摩尔质量、生成二氧化碳气体的质量、生成水的质量,
故答案为:A、B、D;
(8)如果将装置中的B、C连接顺序变为C、B,因为碱石灰将同时吸收水蒸气与CO2,得不到二者各自的质量,无法计算C与H的含量,
故答案为:不能达到.因为碱石灰将同时吸收水蒸气与CO2,得不到二者各自的质量,无法计算C与H的含量.
点评 本题考查了利用燃烧法确定有机物分子组成的知识,为高频考点,侧重于学生的分析、实验和计算能力的考查,难度不大,根据原子守恒法来求解有机物分子组成解答,难度中等,关键在于理解实验原理.


科目:高中化学 来源: 题型:推断题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Na+)+c(H+)=c(X-)+c(OH-) | |
| B. | c(HX)+c(X-)=c(Na+) | |
| C. | 若混合液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) | |
| D. | 若混合液呈酸性,则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含金属元素的离子不一定是阳离子 | |
| B. | 一种元素可形成多种离子,但只能是带同种电荷的离子 | |
| C. | 由同种元素组成的物质肯定属于纯净物 | |
| D. | 具有相同质子数的粒子都属于同种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知二氧化硫可使高锰酸钾溶液褪色反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4
已知二氧化硫可使高锰酸钾溶液褪色反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有③④ | B. | 只有①② | C. | 只有① | D. | 只有②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 步骤 | 实验方案 | 预期现象和结论 |
| ① | 用药匙取少许样品粉末,加入试管A中,再用胶头滴管取过量的NaOH溶液加入试管A中,充分反应后,静置.弃去上层清液,剩余固体备用. | 粉末部分溶解,并有气体放出,则合金中一定含有铝 |
| ② | 向试管A的剩余固体中加入过量的稀硫酸充分反应后,静置,取上层清液于试管B中,剩余固体备用. | 固体部分溶解,并有气体放出,溶液呈浅绿色,则合金中可能含有 铁. |
| ③ | 在试管B中加入少许稀硝酸,再滴加KSCN溶液 | 溶液先变成黄色,加KSCN后显血红色,结合②可知,一定含铁 |
| ④ | 往②剩余固体中加入稀硝酸,再滴加NaOH溶液 | 固体溶解,有无色刺激性气体产生并很快变成红棕色,溶液显蓝色,加NaOH溶液后有蓝色沉淀产生,则合金中一定含有铜. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com