
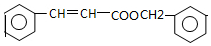 .
.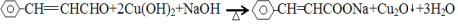 .
.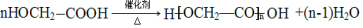 .
. .
.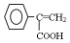 ,写出以
,写出以 为有机原料,制取H的合成路线(可任选无机原料).
为有机原料,制取H的合成路线(可任选无机原料).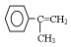 →
→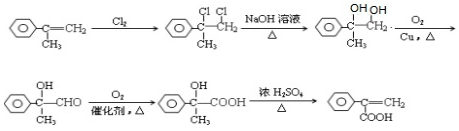 .
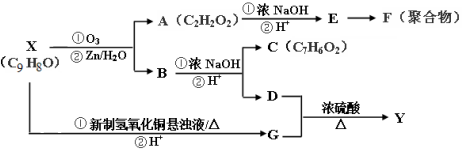
. 分析 根据题中各物质的转化关系结合题中的信息可知,A为OHCCHO,E为HOCH2COOH,E发生脱水缩合生成F( ),C9H8O的不饱和度为6,分子中含有苯环,该物质能与新制氢氧化铜发生反应,说明含有醛基,能被臭氧氧化,说明含有碳碳双键,所以C9H8O结构简式为:
),C9H8O的不饱和度为6,分子中含有苯环,该物质能与新制氢氧化铜发生反应,说明含有醛基,能被臭氧氧化,说明含有碳碳双键,所以C9H8O结构简式为: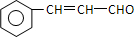 ,X(
,X(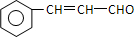 )发生氧化反应生成B(
)发生氧化反应生成B(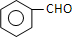 )和A(OHCCHO),B(
)和A(OHCCHO),B( )自身发生反应生成C(
)自身发生反应生成C(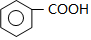 )和D(
)和D(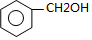 ),X(
),X(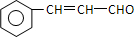 )与新制氢氧化铜、H+等发生反应生成G(
)与新制氢氧化铜、H+等发生反应生成G(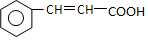 ),D(
),D( )与G(
)与G(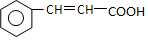 )发生酯化反应生成Y(
)发生酯化反应生成Y(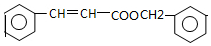 ),据此解答.
),据此解答.
解答 解:(1)X为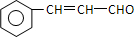 ,由结构简式可知有机物含有碳碳双键、醛基;
,由结构简式可知有机物含有碳碳双键、醛基;
故答案为:碳碳双键、醛基;
(2)D( )与G(
)与G(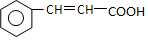 )发生酯化反应生成Y(
)发生酯化反应生成Y(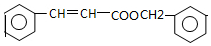 );
);
故答案为: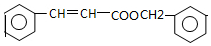 ;
;
(3)D( )与G(
)与G(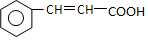 )生成Y(
)生成Y(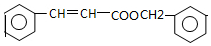 ),是酸与醇的反应,是酯化反应,也属于取代反应;
),是酸与醇的反应,是酯化反应,也属于取代反应;
故答案为:酯化反应(取代反应);
(4) 是醇,能与钠、氢溴酸、乙酸发生取代反应,不显酸性,不能与碳酸钠溶液反应;
是醇,能与钠、氢溴酸、乙酸发生取代反应,不显酸性,不能与碳酸钠溶液反应;
故选c.
(5)X(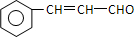 )与新制氢氧化铜第①步反应生成
)与新制氢氧化铜第①步反应生成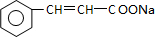 和氧化亚铜,方程式为:
和氧化亚铜,方程式为: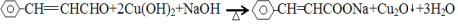 ;
;
E(HOCH2COOH)发生脱水缩合生成F( ),方程式为:
),方程式为: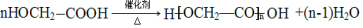 ;
;
故答案为: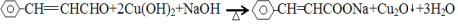 ;
;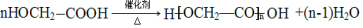 ;
;
(6)C9H8O2的不饱和度为6,分子中含有苯环,苯环的不饱和度为4,能发生银镜反应,能发生水解反应说明分子中含有甲酸某酯;苯环上只有一个取代基
由不饱和度可知,取代基上含有1个碳碳双键,结构简式为: ;
;
故答案为: ;
;
(7) 发生加成反应生成
发生加成反应生成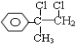 ,
, 进一步发生水解反应生成
进一步发生水解反应生成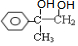 ,接着
,接着 发生氧化反应生成
发生氧化反应生成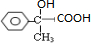 ,最后发生消去反应生成
,最后发生消去反应生成 ,合成路线为:
,合成路线为: ,
,
故答案为: .
.
点评 本题考查有机物的合成、有机反应类型、限制条件同分异构体书写、官能团的结构与性质,注意利用转化关系中隐含的反应设计合成路线,较好的考查学生信息获取与对知识迁移运用,题目难度中等.


科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol/L | B. | 0.05mol/L | C. | 0.4mol/L | D. | 0.01mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室应将钠保存在煤油中 | |
| B. | 分液漏斗和容量瓶在使用前都要检漏 | |
| C. | 可用酒精代替CCl4萃取碘水中的碘单质 | |
| D. | 金属镁失火不可用水来灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
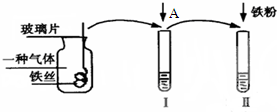 如图是某次实验探究铁及其化合物性质的流程图:
如图是某次实验探究铁及其化合物性质的流程图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com