
”¾ĢāÄæ”æijĪŽÉ«Ļ”ČÜŅŗXÖŠ£¬æÉÄÜŗ¬ÓŠČē±ķĖłĮŠĄė×ÓÖŠµÄij¼øÖÖ”£
ŅõĄė×Ó | CO |
ŃōĄė×Ó | Al3£«”¢Fe3£«”¢Mg2£«”¢NH |
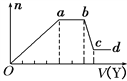
Č”øĆČÜŅŗŹŹĮ棬ĻņĘäÖŠ¼ÓČėijŹŌ¼ĮY£¬²śÉś³ĮµķµÄĪļÖŹµÄĮæ(n)Óė¼ÓČėŹŌ¼ĮĢå»ż(V)µÄ¹ŲĻµČēĶ¼ĖłŹ¾”£
£Ø1£©ČōYŹĒŃĪĖį£¬ŌņČÜŅŗÖŠŗ¬ÓŠµÄŃōĄė×ÓŹĒ______ £¬ab¶Ī·¢Éś·“Ó¦µÄ×ÜĄė×Ó·½³ĢŹ½ĪŖ____________, Oa¶ĪÉĻ±ķÖŠ²Ī¼Ó·“Ó¦µÄĄė×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ________________________”£
[ŅŖ±źĆ÷Ąė×Ó·ūŗÅ£¬Čēn£ØFe3+£©]£®
£Ø2£©ČōYŹĒNaOHČÜŅŗ£¬ŌņXÖŠŅ»¶Øŗ¬ÓŠÉĻ±ķÖŠµÄĄė×ÓŹĒ________________________£¬ĖüĆĒµÄĄė×ÓøöŹż±ČĪŖ______________________________£¬[°“ŃōĄė×ÓŌŚĒ°£¬ŅõĄė×ÓŌŚŗó£¬øß¼ŪŌŚĒ°£¬µĶ¼ŪŌŚŗóµÄĖ³ŠņÅÅĮŠ]£®ab¶Ī·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________£¬ bc¶Ī·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____________________________________”£
”¾“š°ø”æ Na+ 2H£«£«CO32”Ŗ=H2O£«CO2”ü n(AlO2”Ŗ)”Ćn(SiO32”Ŗ)£½2”Ć11 Al3£«”¢Mg2£«”¢NH4£«”¢Cl£ 2:1£ŗ4:12 NH4£«£«OH£=NH3”¤H2O Al(OH)3+OH-=AlO2-+2H2O
”¾½āĪö”æŹŌĢā·ÖĪö£ŗČÜŅŗĪŽÉ«ĖµĆ÷ČÜŅŗÖŠ²»ŗ¬Fe3£«£»
£Ø1£©Čē¹ūYŹĒŃĪĖį£¬ĻņČÜŅŗÖŠ¼ÓŃĪĖį£¬ĻČÉś³É³Įµķ£¬µ±a-b¶ĪŹ±£¬³ĮµķµÄĮæ²»±ä»Æ£¬ŃĪĖįŗĶĢ¼ĖįøłĄė×Ó·“Ӧɜ³ÉĘųĢåĖµĆ÷ČÜŅŗÖŠŗ¬ÓŠCO32”Ŗ£¬ŌņČÜŅŗÖŠ²»ŗ¬Ć¾Ąė×Ó”¢ĀĮĄė×Ó£»µ±b-c¶ĪŹ±³ĮµķµÄÖŹĮæ¼õÉŁ£¬²æ·Ö³ĮµķŗĶŃĪĖį·“Ó¦£¬²æ·Ö³ĮµķŗĶŃĪĖį²»·“Ó¦£¬ĖµĆ÷ČÜŅŗÖŠÓŠ¹čĖįøłĄė×ÓŗĶĘ«ĀĮĖįøłĄė×Ó£¬ČõĖįøłĄė×ÓŗĶļ§øłĄė×ÓÄÜĖ«Ė®½ā£¬ĖłŅŌČÜŅŗÖŠŗ¬ÓŠµÄŃōĄė×ÓŹĒÄĘĄė×Ó£»
£Ø2£©ČōYŹĒĒāŃõ»ÆÄĘ£¬ĻņČÜŅŗÖŠ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬ĻČÉś³É³Įµķ£¬µ±a-b¶ĪŹ±£¬³ĮµķµÄĮæ²»±ä»Æ£¬Ōņa-b¶ĪµÄ·“Ó¦ŹĒĒāŃõ»ÆÄĘŗĶļ§øłĄė×Ó·“Ӧɜ³ÉĘųĢ壻 b-c¶ĪŹ±³ĮµķµÄÖŹĮæ¼õÉŁ£¬²æ·Ö³ĮµķŗĶĒāŃõ»ÆÄĘ·“Ó¦£¬²æ·Ö³Įµķ²»·“Ó¦£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶ØÓŠĀĮĄė×ÓŗĶĆ¾Ąė×Ó£¬ŌņČÜŅŗÖŠ²»ŗ¬¹čĖįøłĄė×Ó”¢Ģ¼ĖįøłĄė×ÓŗĶĘ«ĀĮĖįøłĄė×Ó£¬ĖłŅŌČÜŅŗÖŠŗ¬ÓŠµÄŅõĄė×ÓŹĒĀČĄė×Ó£®
½āĪö£ŗøł¾ŻŅŌÉĻ·ÖĪö£¬ČÜŅŗÖŠŗ¬ÓŠµÄŃōĄė×ÓŹĒÄĘĄė×Ó£¬ab¶Ī·¢Éś·“Ó¦ŹĒĢ¼ĖįøłĄė×ÓŗĶĒāĄė×Ó·“Ӧɜ³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗCO32-+2H+=H2O+CO2”ü£»øł¾ŻĶ¼ĻóÖŖ£¬ĒāŃõ»ÆĀĮŗĶŃĪĖį·“Ó¦ŠčŅŖ1vŃĪĖį£¬Ę«ĀĮĖįøłĄė×ÓŗĶ¹čĖįøłĄė×ÓŗĶŃĪĖį·“Ó¦ŠčŅŖ4VŃĪĖį£¬ÓŠ¹Ų·“Ó¦·½³ĢŹ½ĪŖ£ŗAlO2-+H++H2O=Al£ØOH£©3”ż”¢SiO32-+2H+=H2SiO3”ż”¢Al£ØOH£©3+3H+=Al3++3H2O£¬øł¾Ż·½³ĢŹ½ÖŖ£¬ÓėAlO2-Éś³ÉAl£ØOH£©3ŠčŅŖŃĪĖįµÄĢå»żĪŖ![]() £¬SiO32-Éś³ÉH2SiO3ŠčŅŖŃĪĖįµÄĢå»żŹĒ
£¬SiO32-Éś³ÉH2SiO3ŠčŅŖŃĪĖįµÄĢå»żŹĒ![]() £¬AlO2-”¢SiO32-Éś³É³ĮµķŠčŅŖµÄŃĪĖįĢå»ż±ČŹĒ1:11£¬n(AlO2”Ŗ)”Ćn(SiO32”Ŗ)£½2”Ć11£»
£¬AlO2-”¢SiO32-Éś³É³ĮµķŠčŅŖµÄŃĪĖįĢå»ż±ČŹĒ1:11£¬n(AlO2”Ŗ)”Ćn(SiO32”Ŗ)£½2”Ć11£»
£Ø2£©YŹĒĒāŃõ»ÆÄĘ£¬ĻņČÜŅŗÖŠ¼ÓĒāŃõ»ÆÄĘČÜŅŗ£¬ĻČÉś³É³Įµķ£¬µ±a-b¶ĪŹ±£¬³ĮµķµÄĮæ²»±ä»Æ£¬Ōņa-b¶ĪµÄ·“Ó¦ŹĒĒāŃõ»ÆÄĘŗĶļ§øłĄė×Ó·“Ӧɜ³ÉĘųĢ壻µ±b-c¶ĪŹ±³ĮµķµÄÖŹĮæ¼õÉŁ£¬ĖłŅŌb-c¶ĪŹĒĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖAl£ØOH£©3+OH-=AlO2-+2H2O£¬²æ·Ö³Įµķ²»·“Ó¦£¬ĖµĆ÷ČÜŅŗÖŠŅ»¶ØÓŠĀĮĄė×ÓŗĶĆ¾Ąė×Ó£¬ŌņČÜŅŗÖŠ²»ŗ¬¹čĖįøłĄė×Ó”¢Ģ¼ĖįøłĄė×ÓŗĶĘ«ĀĮĖįøłĄė×Ó£¬øł¾ŻµēŗÉŹŲŗć£¬ČÜŅŗÖŠŗ¬ÓŠµÄŅõĄė×ÓŹĒĀČĄė×Ó£»o-a¶ĪµÄ·“Ó¦ŹĒĀĮĄė×ÓŗĶĆ¾Ąė×ÓÓėĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆĆ¾³Įµķ”£ļ§øłĄė×ÓŠčŅŖĒāŃõ»ÆÄʵÄĢå»żŹĒ2v£¬ĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆÄĘ·“Ó¦ŠčŅŖĒāŃõ»ÆÄʵÄĢå»żŹĒ1v£¬ŌņÉś³ÉĒāŃõ»ÆĀĮŠčŅŖĒāŃõ»ÆÄʵÄĢå»żŹĒ3V£¬Éś³ÉĒāŃõ»ÆĆ¾ŠčŅŖĒāŃõ»ÆÄʵÄĢå»żŹĒ4v-3v=1V£¬Ōņn£ØAl3+£©£ŗn£ØMg2+£©£ŗn£ØNH4+£©=1£ŗ![]() £ŗ2=2£ŗ1£ŗ4£¬øł¾ŻČÜŅŗÖŠŅõŃōĄė×ÓĖł“ųµēŗÉĻąµČÖŖ£¬n£ØAl3+£©£ŗn£ØMg2+£©£ŗn£ØNH4+£©”¢n£ØCl-£©=2£ŗ1£ŗ4£ŗ12£¬¼“N£ØAl3+£©£ŗN£ØMg2+£©£ŗN£ØNH4+£©”¢N£ØCl-£©=2£ŗ1£ŗ4£ŗ12£»a-b¶ĪµÄ·“Ó¦ŹĒĒāŃõ»ÆÄĘŗĶļ§øłĄė×Ó·“Ӧɜ³É°±Ęų£¬Ąė×Ó·½³ĢŹ½ŹĒNH4£«£«OH£=NH3”¤H2O£»b-c¶ĪŹĒĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬·“Ó¦Ąė×Ó·½³ĢŹ½ŹĒAl(OH)3+OH-=AlO2-+2H2O”£
£ŗ2=2£ŗ1£ŗ4£¬øł¾ŻČÜŅŗÖŠŅõŃōĄė×ÓĖł“ųµēŗÉĻąµČÖŖ£¬n£ØAl3+£©£ŗn£ØMg2+£©£ŗn£ØNH4+£©”¢n£ØCl-£©=2£ŗ1£ŗ4£ŗ12£¬¼“N£ØAl3+£©£ŗN£ØMg2+£©£ŗN£ØNH4+£©”¢N£ØCl-£©=2£ŗ1£ŗ4£ŗ12£»a-b¶ĪµÄ·“Ó¦ŹĒĒāŃõ»ÆÄĘŗĶļ§øłĄė×Ó·“Ӧɜ³É°±Ęų£¬Ąė×Ó·½³ĢŹ½ŹĒNH4£«£«OH£=NH3”¤H2O£»b-c¶ĪŹĒĒāŃõ»ÆĀĮŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬·“Ó¦Ąė×Ó·½³ĢŹ½ŹĒAl(OH)3+OH-=AlO2-+2H2O”£


 ¾ŁŅ»·“ȿʌĩ°Ł·Ö³å“Ģ¾ķĻµĮŠ“š°ø
¾ŁŅ»·“ȿʌĩ°Ł·Ö³å“Ģ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£ØNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ£©£Ø £©
A.71gĀČĘųŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖNA
B.4 g½šŹōøʱä³ÉøĘĄė×ÓŹ±Ź§Č„µÄµē×ÓŹżÄæĪŖ0.1NA
C.±ź×¼×“æöĻĀ£¬22.4LH2OÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA
D.ŌŚ±ź×¼×“æöĻĀ£¬22.4 L¼×ĶéÓėŅŅČ²µÄ»ģŗĻĪļĖłŗ¬·Ö×ÓŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĪļÖŹÄÜĻą»„·“Ó¦µĆµ½Al(OH)3µÄŹĒ
A. ĀĮøśNaOHČÜŅŗ
B. Al(NO3)3øś¹żĮæµÄNaOHČÜŅŗ
C. Al2O3ŗĶČČĖ®
D. Al2(SO4)3ČÜŅŗøś¹żĮæµÄ°±Ė®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖŅŌ»ĘĶæóŗĶĮņ»ĒĪŖŌĮĻÖĘČ”ĶŗĶĘäĖū²śĪļµÄŠĀ¹¤ŅÕ£¬ŌĮĻµÄ×ŪŗĻĄūÓĆĀŹ½Ļøߣ®ĘäÖ÷ŅŖĮ÷³ĢČēĻĀ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ 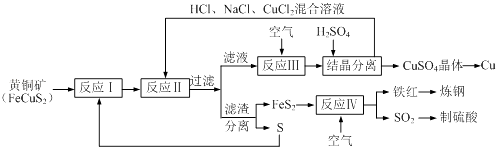
£Ø1£©·“Ó¦¢óµÄĄė×Ó·½³ĢŹ½ĪŖ4CuCl2©+O2+4H+ØT4Cu2++8Cl©+2H2O£¬CuCl2©ÖŠĶŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ £¬ øĆ·“Ó¦ÖŠµÄŃõ»Æ¼ĮŹĒ £®
£Ø2£©Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚ·“Ó¦¢óĖłµĆµÄČÜŅŗÖŠ¼ÓČėĮņĖį£¬æÉŅŌĪö³öĮņĖįĶ¾§Ģå¶ų²»Īö³öĀČ»ÆĶ¾§Ģ壬ĘäŌŅņæÉÄÜŹĒ £®
£Ø3£©Į¶øÖŹ±£¬æɽ«ĢśŗģĶ¶ČėČŪČŚµÄÉśĢśÖŠ£¬ŅŌ½µµĶÉśĢśµÄŗ¬Ģ¼Į棬øĆ¹ż³ĢÖŠÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ £®
£Ø4£©SO2Ī²ĘųÖ±½ÓÅŷŵ½“óĘųÖŠŌģ³É»·¾³ĪŪČ¾µÄŗó¹ūŹĒ £®
£Ø5£©ŅŃÖŖ·“Ó¦¢ņµÄĄė×Ó·½³ĢŹ½ĪŖCu2++CuS+4Cl©ØT2CuCl2©+S£¬·“Ó¦¢ńµÄ²śĪļĪŖŗĶ £® £ØĢī»ÆѧŹ½£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»ÆŹĒÓÉ»Æѧ·“Ó¦ÖŠ¾É»Æѧ¼ü¶ĻĮŃŹ±ĪüŹÕµÄÄÜĮæÓėŠĀ»Æѧ¼üŠĪ³ÉŹ±·Å³öµÄÄÜĮæ²»Ķ¬ŅżĘšµÄ£®ČēĶ¼ĪŖN2£Øg£©ŗĶO£Øg£©·“Ӧɜ³ÉNO£Øg£©¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£ŗĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £© 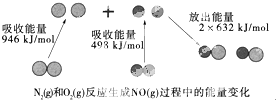
A.1 mol N2£Øg£©ŗĶ1 mol O2£Øg£©·“Ó¦·Å³öµÄÄÜĮæĪŖ180 kJ
B.1 mol N2£Øg£©ŗĶ1 mol O2£Øg£©¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2 mol NO£Øg£©¾ßÓŠµÄ×ÜÄÜĮæ
C.Ķس£ĒéæöĻĀ£¬N2£Øg£©ŗĶO2£Øg£©»ģŗĻÄÜÖ±½ÓÉś³ÉNO
D.NOŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æX”¢Y”¢Z”¢W“ś±ķ¶ĢÖÜĘŚµÄĖÄÖÖŌŖĖŲ£¬ÓŠ¹ŲĖüĆĒµÄ²æ·ÖŠÅĻ¢Čē±ķĖłŹ¾£ŗ
ŌŖĖŲ | ²æ·Ö½į¹¹ĢŲµć | ²æ·ÖŠŌÖŹ |
X | XµÄµ„ÖŹÓÉĖ«Ō×Ó·Ö×Ó¹¹³É£¬·Ö×ÓÖŠÓŠ14 | XÓŠ¶ąÖÖŃõ»ÆĪļ£¬ČēXO”¢XO2µČ |
Y | YŌ×ӵēĪĶā²ćµē×ÓŹżµČÓŚ×īĶā²ćµē×ÓŹż | YŌŖĖŲÄÜŠĪ³É¶ąÖÖµ„ÖŹ |
Z | ZŌ×ÓµÄ×īĶā²ćµē×ÓŹż¶ąÓŚ4 | ZŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼ŪÓė×īµĶøŗ»ÆŗĻ¼ŪµÄ“śŹżŗĶµČÓŚ6 |
W | µŚČżÖÜĘŚŌŖĖŲµÄ¼ņµ„Ąė×ÓÖŠ°ė¾¶×īŠ” | WµÄµ„ÖŹ»ÆѧŠŌÖŹĖä½Ļ»īĘĆ£¬µ«Ö»Šč³£ĪĀ±£“ę |
Ēė°“ŅŖĒó»Ų“šĻĀĮŠĪŹĢā£Ø×¢Ņā²»ÄÜÓĆ×ÖÄøX”¢Y”¢Z”¢W×÷“š£¬ĒėÓĆĻąÓ¦µÄŌŖĖŲ·ūŗÅ»ņ»ÆѧŹ½ĢīŠ“£©£ŗ
£Ø1£©XµÄŌŖĖŲĆū³ĘŹĒ£¬XµÄĘųĢ¬Ēā»ÆĪļµÄµē×ÓŹ½ŹĒ £®
£Ø2£©ZŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆŹĒµŚÖÜĘŚ£¬µŚ×壮ZŗĶWŠĪ³ÉµÄ»ÆŗĻĪļŹōÓŚ»ÆŗĻĪļ£ØĢī”°Ąė×Ó”±»ņ”°¹²¼Ū”±£©£®
£Ø3£©X”¢Y”¢Z”¢WµÄŌ×Ó°ė¾¶“ӓ󵽊”µÄĖ³ŠņŹĒ £®
£Ø4£©X”¢Y”¢ZČżÖÖŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌÓÉĒæµ½ČõµÄĖ³ŠņŹĒ£ŗ £®
£Ø5£©ĶŗĶXµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄÅØČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ £®
£Ø6£©ĘųĢå·Ö×Ó£ØYX£©2³ĘĪŖÄāĀ±ĖŲ£¬ŠŌÖŹÓėĀ±ĖŲĄąĖĘ£¬ĒėŠ“³ö£ØYX£©2ÓėNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. æÉÓƱ½ŻĶČ”ĖÄĀČ»ÆĢ¼ÖŠµÄµā
B. ±½µĪČėäåĖ®ÖŠ£¬·¢ÉśČ”“ś·“Ӧɜ³Éäå±½
C. æÉÓĆŹÆČļŹŌŅŗĒų·ÖŅŅ“¼ŗĶŅŅĖįĮ½ÖÖĪļÖŹ
D. µČĪļÖŹµÄĮæµÄ¼×ĶéÓėĀČĘų»ģŗĻ¹āÕÕÖĮ³ä·Ö·“Ó¦£¬²śĪļÖŠ×ī¶ąŹĒĖÄĀČ»ÆĢ¼
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĪĀøßŃ¹ĻĀ£¬1LĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśČēĻĀ·“Ó¦£ŗ2H2+COCH3OH£®·“Ó¦æŖŹ¼Ź±H2µÄĪļÖŹµÄĮæĪŖ5mol£¬5minŹ±±äĪŖ0.5mol£¬Ōņ5minÄŚøĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2£©£Øµ„Ī»£ŗmolL©1min©1£©ĪŖ£Ø £©
A.9.0
B.0.9
C.0.45
D.4.5
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±ķŹĒŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬øł¾ŻĖłøųµÄ10ÖÖŌŖĖŲ£¬Ķź³ÉŅŌĻĀø÷Š”Ģā£®
×å | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0 |
2 | C | N | O | Ne | ||||
3 | Na | Mg | Al | Si | S | Cl |
£Ø1£©Ć¾µÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ £®
£Ø2£©H2SO4ÓėHClO4ÖŠ£¬ĖįŠŌ½ĻĒæµÄŹĒ £®
£Ø3£©NaOHÓėAl£ØOH£©3ÖŠ£¬ŹōÓŚĮ½ŠŌĒāŃõ»ÆĪļµÄŹĒ £¬ Ėü³£ÓĆ×÷ÖĪĮĘĪøĖį£Øŗ¬ŃĪĖį£©¹ż¶ąµÄŅ©Īļ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £®
£Ø4£©Ģ¼ŌŖĖŲŠĪ³ÉµÄŅ»ÖÖŃõ»ÆĪļµÄ»ÆѧŹ½ŹĒ £¬ øĆĪļÖŹÖŠCŌŖĖŲÓėOŌŖĖŲµÄÖŹĮæ±ČĪŖ £® £ØĻą¶ŌŌ×ÓÖŹĮæ£ŗC©12 O©16£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com